
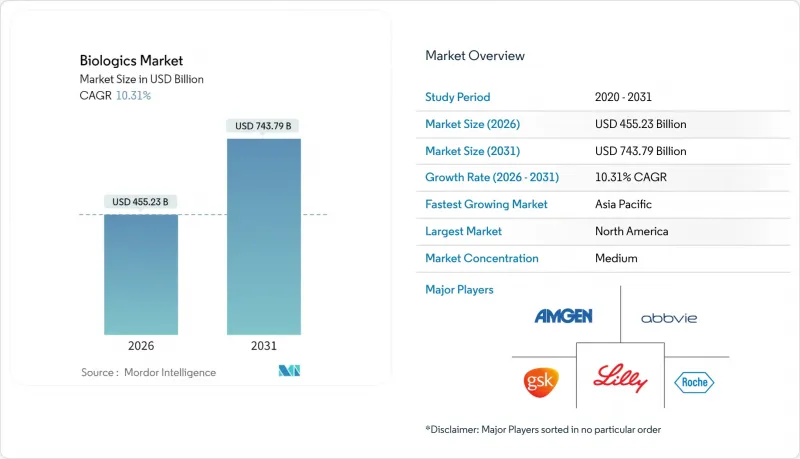
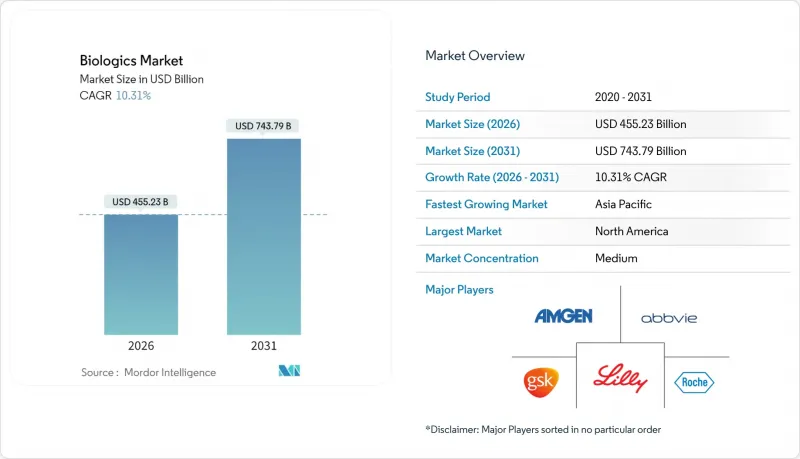
바이오로직스 시장은 2025년에 4,126억 8,000만 달러로 평가되며, 2026년 4,552억 3,000만 달러에서 2031년까지 7,437억 9,000만 달러에 달할 것으로 예측됩니다.
예측 기간(2026-2031년)의 CAGR은 10.31%로 예상됩니다.
정밀항암제, 차세대 모노클로널 항체, 유전자치료제에 대한 강력한 수요가 이러한 성장을 촉진하고 있습니다. 만성질환의 유병률 증가, 규제 지정의 가속화, 지속적인 벤처 자금 지원으로 인해 이러한 복잡한 치료법은 연구 단계에서 일상적인 치료로 계속 이동하고 있습니다. 2024년 이후 150억 달러 이상의 제조 투자로 노스캐롤라, 덴마크, 독일에 새로운 생산 능력을 구축하여 생산자들은 최근 공급 병목 현상을 완화하기 위한 준비를 하고 있습니다. 동시에, 혁신 기업은 연속관류법이나 일회용 바이오리액터를 채택하여 속도와 초기 비용 절감을 동시에 실현하고 있습니다. 한편, 지불자는 지출을 억제하기 위해 바이오시밀러의 채택을 확대하고 있습니다.
암, 자가면역질환, 대사성 질환은 복잡한 병태생리 경로를 보여 저분자 의약품으로는 완벽한 대응이 어려운 질환입니다. 면역요법이 초기 치료 라인으로 이동하는 가운데, 바이오로직스의 종양학 분야에서의 사용은 36.54%의 점유율을 차지하며 13.78%의 연평균 복합 성장률(CAGR)을 기록했습니다. 신규 B세포 고갈 항체를 이용한 류마티스 관절염 치료에서 87%의 증상 악화 억제가 보고되어 우수한 임상적 관리 효과가 입증되었습니다. 당뇨병 및 비만 치료용 GLP-1 작용제는 공급보다 수요가 많아 노보 노디스크는 새로운 충전 및 마무리 시설에 41억 달러를 투자하기로 결정했습니다. 희귀질환 치료제는 희귀의약품으로 지정되어 프리미엄 가격 책정이 가능한 특혜를 받고 있으며, 바이오의약품 시장 내에서 작지만 수익성이 높은 틈새 시장을 다수 창출하고 있습니다.
FDA의 간소화된 대체가능성 지침에 따라 바이오시밀러 개발 기업은 분석적 동일성이 입증되면 전환 시험을 생략할 수 있습니다. RMAT(재생의료 첨단치료제) 및 혁신치료제 지정으로 2024년 승인된 7개의 세포-유전자치료제(흑색종 치료제 리피루셀, 혈우병 B 치료제 피다나코젠 엘라파보벡 등)의 승인 절차가 단축되었습니다. EMA(유럽의약품청)가 미국 정책과 일치함에 따라 대서양을 가로지르는 동시 출시가 가능해져 중복 비용을 절감할 수 있게 되었습니다. 중국 국가약품감독관리총국은 심사 프로세스를 개선하여 아케소가 이보네시맙이 세계 표준을 능가하는 데이터로 조기 승인을 받을 수 있도록 했습니다. 이를 통해 바이오로직스 시장에서의 경쟁력을 강화할 수 있습니다.
바이오의약품 공장 1기 건설에는 10억 달러 이상의 자본이 필요하며, 노보노디스크의 클레이튼 확장 프로젝트와 일라이 릴리의 30억 달러 규모의 위스콘신 공장이 그 실례입니다. 1회용 시스템으로 공사기간은 단축되었지만, 잦은 백 교체와 특수 배지가 운영비용을 증가시켰습니다. 엔드 투 엔드 프로그램은 10-15년에 진행되며, 시험 비용만 3억 달러에 달할 수 있으며, 소규모 바이오텍 기업의 진입을 제한하고 있습니다. CHO 배지, 수지, 멸균 주사기 공급 병목현상은 비용을 높이고 일정을 위협합니다. 스케일업시 일탈은 제품의 무결성을 해칠 위험이 있으므로 엄격한 프로세스 검증이 필수적이며, 이는 막대한 비용이 소요됩니다.
모노클로널 항체는 2025년 2,720억 9,000만 달러(바이오의약품 시장 규모의 65.92%)를 차지할 것으로 예상되며, 수십년에 걸친 제조 기술 발전의 혜택을 누리고 있습니다. 이 카테고리는 종양학, 자가면역질환, 염증성 질환에 적용되며, 예측 가능한 약리학적 특성이 폭넓은 지불자 수용을 지원하고 있습니다. 한편, 유전자 기반 바이오로직스는 혈우병 및 유전성 망막질환에 대한 최초 승인에 힘입어 2031년까지 연평균 12.11%의 성장률을 보일 것으로 예측됩니다. 백신은 정부의 팬데믹 대응 자금으로 인해 안정적 기둥을 유지하고 있는 반면, 재조합 단백질은 성숙한 바이오시밀러로 인해 가격 하락 압력에 직면해 있습니다.
개발 파이프라인에 대한 투자는 세포 기반 치료제에 집중되고 있으며, 2024년 7건의 신규 FDA 승인은 동종 CAR-T 치료제와 줄기세포 제품을 입증한 것을 증명하고 있습니다. 항체-약물 접합체(ADC)와 다중특이적 항체는 표적 도메인과 세포독성 및 면역조절 페이로드를 융합하여 정밀 암 치료의 폭을 넓히고 있습니다. 현재 250개 이상의 단백질 엔지니어링 프로그램이 반감기, 조직 침투성, 면역원성 프로파일을 최적화하기 위해 노력하고 있습니다. 이러한 변화는 바이오로직스 시장 가치를 향상시키고 치료 범위를 확대하여 지속적인 두 자릿수 성장을 지원하고 있습니다.
2025년 기준 바이오로직스 시장 규모의 36.12%를 차지하는 종양학 분야는 체크포인트 억제제, ADC, CAR-T 치료제의 급속한 보급을 반영하여 13.45%의 연평균 복합 성장률(CAGR)을 보일 것으로 예측됩니다. 이어 자가면역질환 분야에서는 차세대 이중특이성항체가 TNF 억제제에 비해 우수한 질병 조절 효과를 보이고 있습니다. 감염병 생물학은 예방 백신에서 더 나아가 바이러스나 세균의 위협에 대한 노출 후 치료제로 확대되고 있습니다.
대사 및 내분비 질환 분야에서는 GLP-1 작용제가 만성 체중 관리에 대한 적응증 확대로 규모를 확대하며 150억 달러 이상의 세계 생산 능력 프로젝트를 주도하고 있습니다. 안과 영역에서는 단회 투여로 지속적인 효과를 내는 유전자 치료제가 성장의 열쇠가 될 것입니다. 희귀질환 파이프라인은 희귀질환 치료제 우대정책으로 대상 환자층 확대. 다양한 적응증이 결합되어 특정 영역이 침체되더라도 바이오로직스 시장의 회복력을 강화할 수 있습니다.
북미는 2025년 바이오로직스 시장 점유율 39.98%로 1위를 유지. 탄탄한 상환제도, 풍부한 벤처캐피털, 획기적 치료제 지정 속도를 높이는 FDA가 지원하고 있습니다. 이 지역에는 150억 달러 이상의 신규 생산능력에 대한 투자가 이루어졌으며, 리서치 트라이앵글 지역은 노보노디스크, 일라이 릴리, 암젠을 중심으로 한 세계 거점으로 변모하고 있습니다. 보급률이 성숙해짐에 따라 성장률은 CAGR 9.56%로 둔화될 것이며, 바이오시밀러의 보급에 따른 경쟁 심화가 예상됩니다.
아시아태평양은 11.32%의 가장 빠른 CAGR을 달성했습니다. 중국, 일본, 인도는 규제 프로세스를 정비하고 바이오 제조에 투자하고 있습니다. 중국의 신속한 승인 절차로 인해 국내 기업이 혁신적인 암 치료용 바이오의약품을 출시하며 유럽과 미국의 기존 기업에게 도전장을 내밀고 있습니다. 일본에서는 세제 혜택과 공적 자금을 활용하여 번역 연구를 지원하고 있습니다. 한편, 한국의 삼성바이오로직스는 CDMO 역량을 전 세계에 수출하고 있습니다. 인도는 바이오시밀러 및 초기 단계 프로젝트를 위해 저비용의 인력을 활용하여 이 지역에서의 입지를 더욱 확장하고 있습니다.
유럽은 성숙한 바이오시밀러 프레임워크와 높은 공공 의료 지출을 배경으로 9.05%의 안정적인 CAGR을 유지하고 있습니다. 독일과 스위스는 복잡한 항체 의약품의 고부가가치 생산을, 아일랜드와 덴마크는 유리한 법인세 제도를 통해 다국적 기업의 진출을 유치하고 있습니다. 고령화와 만성질환의 확산이 기반 수요를 지원하고, EU 전역의 규제 지침 조화가 시장 진입 장벽을 낮추고 있습니다.
The Biologics Market was valued at USD 412.68 billion in 2025 and estimated to grow from USD 455.23 billion in 2026 to reach USD 743.79 billion by 2031, at a CAGR of 10.31% during the forecast period (2026-2031).
Strong demand for precision oncology agents, next-generation monoclonal antibodies, and gene-based therapeutics steers this expansion. Heightened chronic disease prevalence, accelerated regulatory designations, and sustained venture funding continue to move these complex therapies from research pipelines into routine care. Manufacturing investment exceeding USD 15 billion since 2024 builds new capacity in North Carolina, Denmark, and Germany, positioning producers to ease recent supply bottlenecks. At the same time, innovators adopt continuous perfusion and single-use bioreactors to combine speed with lower upfront costs, while payers increasingly embrace biosimilars to contain spending.
Cancer, autoimmune disorders, and metabolic diseases present complex pathways that small-molecule drugs no longer address fully. Oncology uses of biologics command 36.54% share and post a 13.78% CAGR as immunotherapies move into earlier treatment lines. Rheumatoid arthritis patients treated with novel B-cell depletion antibodies report 87% flare reduction, illustrating superior clinical control. GLP-1 agonists for diabetes and obesity have outstripped supply, prompting Novo Nordisk to commit USD 4.1 billion to new fill-finish space. Rare disease therapies enjoy orphan incentives that allow premium pricing, creating many small but profitable niches within the biologics market.
The FDA's streamlined interchangeability guidance lets biosimilar developer s bypass switching studies if analytical sameness is proven. RMAT and breakthrough labels shortened timelines for seven cell and gene therapies cleared in 2024, including lifileucel for melanoma and fidanacogene elaparvovec for hemophilia B. EMA alignment with U.S. policy now delivers simultaneous trans-Atlantic launches, trimming duplication costs. China's National Medical Products Administration has overhauled its process, enabling Akeso to bring ivonescimab forward with data that outperforms global standards and strengthens competitiveness in the biologics market.
A single biologics plant demands capital above USD 1 billion, as illustrated by Novo Nordisk's Clayton expansion and Eli Lilly's USD 3 billion Wisconsin site. Although single-use systems reduced build time, frequent bag changeovers and specialized media lift operating expense. End-to-end programs span 10-15 years and can cost USD 300 million in trials alone, limiting small biotech participation. Supply bottlenecks in CHO media, resins, and sterile syringes inflate costs and threaten scheduling. Any deviation during scale-up risks product integrity, making rigorous process validation essential and expensive.
Other drivers and restraints analyzed in the detailed report include:
For complete list of drivers and restraints, kindly check the Table Of Contents.
Monoclonal antibodies contributed USD 272.09 billion, equal to 65.92% of the biologics market size in 2025, benefiting from decades of manufacturing refinement. The class spans oncology, autoimmune, and inflammatory uses, and its predictable pharmacology supports broad payer acceptance. In contrast, gene-based biologics post a 12.11% CAGR through 2031, propelled by first-in-class approvals for hemophilia and inherited retinal diseases. Vaccines remain a steady pillar as governments fund pandemic readiness, while recombinant proteins face downward price pressure from mature biosimilars.
Pipeline investment tilts toward cell-based modalities, evidenced by seven fresh FDA approvals in 2024 that validated allogeneic CAR-T and stem cell products. ADCs and multispecific antibodies broaden precision oncology by fusing targeting domains with cytotoxic or immune-modulatory payloads. Over 250 protein-engineering programs now optimize half-life, tissue penetration, and immunogenicity profiles. These shifts collectively raise the biologics market value proposition and expand therapeutic range, underwriting sustained double-digit growth.
Oncology accounted for 36.12% of the biologics market size in 2025 and will rise at a 13.45% CAGR, mirroring rapid uptake of checkpoint inhibitors, ADCs, and CAR-T therapies. Autoimmune conditions follow, as next-generation bispecific antibodies demonstrate superior disease control relative to TNF inhibitors. Infectious disease biologics develop beyond prophylactic vaccines into post-exposure therapeutics against viral and bacterial threats.
Metabolic and endocrine disorders add scale as GLP-1 agonists extend indications to chronic weight management, triggering worldwide capacity projects valued above USD 15 billion. Ophthalmology stands to gain from gene therapy that delivers durable benefit after a single administration. Rare disease pipelines, spurred by orphan incentives, deepen the addressable patient pool. Collectively, diversified applications reinforce resilience in the biologics market even if one therapeutic area softens.
The Biologics Market Report is Segmented by Product (Monoclonal Antibodies, Vaccines, and More), Application (Oncology, Autoimmune & Inflammatory, and More), Source (Mammalian Cell-Culture, and More), Manufacturing Technology (Single-Use Bioreactors, and More), End-User (Pharmaceutical & Biotech Companies, and More), and Geography (North America, Europe, and More). The Market Forecasts are Provided in Terms of Value (USD).
North America sustained leadership with 39.98% biologics market share in 2025, buoyed by robust reimbursement, venture capital depth, and an FDA that expedites breakthrough designations. The region channels more than USD 15 billion into new capacity, transforming the Research Triangle into a global hub anchored by Novo Nordisk, Eli Lilly, and Amgen. Although growth moderates to 9.56% CAGR as penetration matures, competitive intensity rises as biosimilars take hold.
Asia-Pacific delivers the quickest 11.32% CAGR as China, Japan, and India refine regulatory pathways and invest in biomanufacturing. China's streamlined approval timeline allows domestic players to launch innovative oncology biologics that challenge Western incumbents. Japan leverages tax incentives and public funding to support translational research, while South Korea's Samsung Biologics exports CDMO capacity globally. India capitalizes on low-cost talent for biosimilar and early-phase projects, further enlarging the region's footprint.
Europe maintains steady 9.05% CAGR on the back of mature biosimilar frameworks and high public health spending. Germany and Switzerland host high-value production for complex antibodies, whereas Ireland and Denmark entice multinational expansions via favorable corporate tax regimes. Aging demographics and chronic disease prevalence sustain underlying demand, and pan-EU harmonization of regulatory guidance reduces market entry friction.