
임상 진단 시장은 2025년 887억 9,000만 달러에서 2026년에는 935억 9,000만 달러로 성장할 것으로 예상되며, 2026년부터 2031년까지 CAGR 5.41%를 기록하며 2031년까지 1,217억 6,000만 달러에 달할 것으로 예측됩니다.
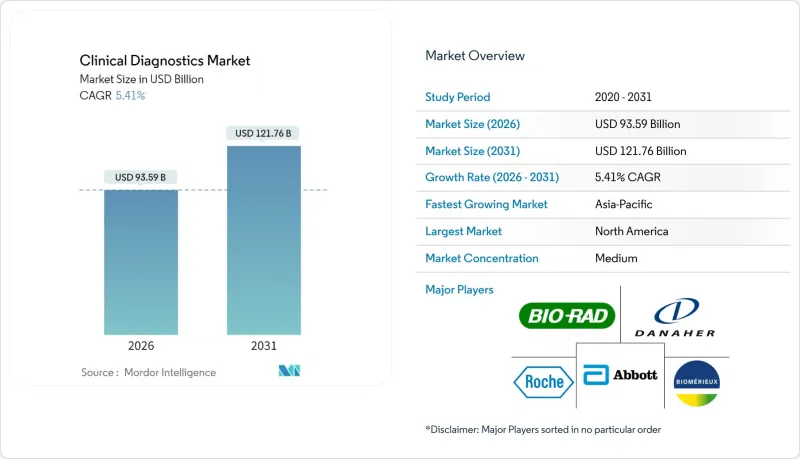
이 전망은 검사실이 자동화, 인공지능, 정밀의료 기능을 통합함에 따라, 전염병으로 인한 변동성에서 꾸준한 성장으로 전환하고 있음을 보여줍니다. 만성질환의 유병률 증가로 인해 일상적인 전혈구(CBC) 검사량은 높은 수준을 유지하고 있지만, 의료시스템이 개인화 의료 모델을 채택함에 따라 종양학 바이오마커 패널에 대한 수요는 더욱 빠르게 증가하고 있습니다. 장비의 자동화로 검사 1회당 시약 소비량이 감소하는 반면, 시약 가격에 대한 압박이 증가하고 있습니다. 또한, 데이터 관리 소프트웨어는 품질 보증과 상호운용성 측면에서 '있으면 편리한 것'에서 '필수적인 것'으로 그 위상이 변화하고 있습니다. 신흥 경제국에서는 분산형 및 재택 검사 형태를 위한 인프라 투자가 진행되고 있으며, 임상 진단 시장은 전통적인 의료기관 기반을 넘어 확대되고 있습니다.
인공지능 모듈은 현재 수백만 건의 익명화된 검사 기록을 분석하여 사람의 눈으로는 간과하기 쉬운 미묘한 진단 패턴을 추출합니다. 퀘스트 다이아그노스틱스의 구글 클라우드와의 제휴를 통해 복잡한 사례의 오진율이 약 30% 감소하고, 응급값 검사 결과 보고 시간도 단축되었습니다. 이에 따라 의료 서비스 제공자들은 AI 기능을 부가 기능이 아닌 표준 인프라로 인식하기 시작했습니다. 의사들이 보다 신속하고 정확한 결과 제공 경로를 원하는 가운데, 초기 도입 업체는 소개 환자 점유율을 더욱 확대하고 있습니다.
가디언트헬스의 종양 프로파일링 검사는 유전체, 단백질체, 메타볼롬 데이터의 다층적 분석이 치료 선택을 정교화하고 생검의 반복을 줄일 수 있는 실례를 보여주고 있습니다. 검사기관은 검체 채취 일정의 통합과 준수율 향상을 통해 초기 비용 증가를 정당화하고, 진단 정확도가 다운스트림 치료 비용 절감에 명확하게 기여하는 가치 기반 보상 체계로의 전환을 지원하고 있습니다.
병원은 전염병의 급증에 대처하기 위해 중복 분자 분석 장비를 구입했지만, 현재 대부분 40-60%의 가동률로 운영되고 있어 새로운 자본 배분이 지연되고 있습니다. Abbott Laboratories는 고객이 플랫폼 업그레이드가 아닌 기존 재고를 소진하기 때문에 2025년 진단 수익이 감소할 것이라고 발표했습니다. 가격 경쟁이 심화되고 마진이 압축되어 대규모 시스템의 경우 교체 주기가 18-24개월로 연장되고 있습니다.
종양학 및 종양표지자 검사는 동반진단 의무화에 따른 의약품 조정을 반영하여 10.39%의 CAGR을 기록할 것으로 예상됩니다. CBC는 2025년 임상 진단 시장에서 24.24%의 점유율을 유지하며, 급성 및 만성질환 치료 경로의 기본 볼륨의 안정성을 유지하고 있습니다.
다항목 암 패널의 확대는 바이오마커를 통합하여 워크플로우의 경제성을 향상시키지만, 지질 프로파일은 일차 의료의 턴어라운드 기준을 충족하는 휴대용 기기로 대체될 위험에 직면해 있습니다. 감염병 검사 메뉴는 팬데믹 당시 높은 수준에서 정상화되었지만, 항균제 내성 감시 프로그램에서는 여전히 중요한 역할을 하고 있습니다.
시약 및 키트는 2025년 매출의 64.98%를 차지할 것으로 예상되며, 데이터 관리 소프트웨어는 실험실의 품질 관리 및 규제 감사 추적의 디지털화가 진행됨에 따라 CAGR 10.62%를 기록할 것으로 예상됩니다. 장비에는 현재 오픈 API가 탑재되어 미들웨어를 통한 샘플 라우팅, 시약 분배, 결과 공개를 실시간으로 조정할 수 있어 설비 투자 억제 하에서 자산 수명 연장을 실현하고 있습니다. 경쟁 입찰로 인해 시약의 수익률이 압박받고 있는 가운데, 벤더들은 물리적 소모품이 아닌 워크플로우 효율화를 통한 고객 로열티 확보를 목적으로 정보학 구독 번들화를 추진하고 있습니다.
북미는 높은 1인당 지출로 인해 2025년 기준 37.98%의 점유율을 유지했지만, 아시아태평양의 10.14%의 CAGR은 의료 접근성 확대와 만성질환 발생률의 증가를 뒷받침하고 있습니다. 아시아태평양에서는 공립병원의 확장, 전국민 의료보험제도 도입, 검사 1인당 비용 절감을 위한 현지 제조 장려책으로 2026년부터 2031년까지 156억 2,000만 달러 이상의 매출 증가가 예상됩니다. 정부 보조금은 지방의 전문의 부족을 완화하는 분산형 플랫폼을 촉진하고, 임상 진단 시장이 새로운 사용자 층을 개척하고 두 자릿수 수량 성장을 견인할 수 있도록 합니다. 다국적 기업들은 현지 당국과 협력하여 수입 관세를 피하고 리드 타임을 단축하기 위해 시약 충전 시설을 설립하고 있습니다.
북미 시장은 성숙한 시장이지만, 여전히 기술 동향의 지표가 되고 있습니다. AI 탑재 분자 패널 검사 및 재택 검체 물류는 통합 의료 네트워크에서 시범 프로그램에서 전체 시스템 지원 프로토콜로 전환되었습니다. 그러나 상환 제한과 사전 승인 의무가 검사 건수 증가를 억제하고 있습니다. 이에 대해 검사기관은 정밀 암 검사와 실제 임상 데이터(RWE)를 결합하여 성과 연동형 계약에서 가치를 정당화하기 위한 노력을 진행하고 있습니다. 지역 의료시스템이 일상 업무를 대규모 검사기관에 위탁하는 움직임이 지속되고 있으며, 규모의 최적화와 차세대 정보 시스템에 대한 투자가 진행되고 있습니다.
유럽에서는 지역마다 다른 추세를 보이고 있습니다. 북유럽 국가들은 예방의료 예산을 심혈관질환 및 대사성 질환 검진에 집중하는 반면, 남유럽 국가들은 재정 긴축으로 인해 고가의 분자검사 도입이 제한되고 있습니다. 유럽연합의 체외진단의료기기 규정(IVDR)은 컴플라이언스 요건을 더욱 강화하고 있으며, 소규모 제조업체들은 수익성이 낮은 제품 라인에서 철수해야 하는 상황에 처해 있습니다. 그럼에도 불구하고 고령화 사회는 안정적인 기준선 수요를 보장하고, 희귀질환 진단에 있어 국경을 초월한 협력이 전문 검사 수요를 뒷받침하고 있습니다.
The clinical diagnostics market is expected to grow from USD 88.79 billion in 2025 to USD 93.59 billion in 2026 and is forecast to reach USD 121.76 billion by 2031 at 5.41% CAGR over 2026-2031.
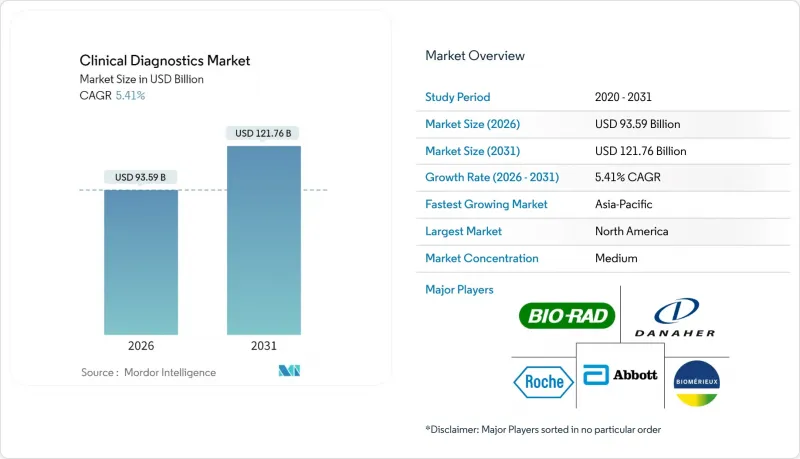
This outlook signals a shift from pandemic-driven volatility to steady growth as laboratories converge automation, artificial intelligence, and precision-medicine capabilities. Heightened chronic-disease prevalence keeps routine Complete Blood Count (CBC) volumes high, yet oncology biomarker panels scale faster as health systems embrace personalized care models. Reagent pricing pressure intensifies as instrument automation trims per-test consumption, while data-management software moves from "nice-to-have" to "mission-critical" status for quality-assurance and interoperability. Emerging economies funnel infrastructure investments toward decentralized and home-based testing formats, expanding the clinical diagnostics market beyond its traditional institutional base.
Artificial-intelligence modules now sift millions of anonymized laboratory records to surface subtle diagnostic patterns that human review often misses. Quest Diagnostics' alliance with Google Cloud cut complex-case error rates by nearly 30% while trimming turnaround times for critical values, prompting providers to view AI capacity as standard infrastructure rather than an add-on. Early adopters further gain referral share as physicians gravitate to faster and more confident result-delivery pathways.
Guardant Health's tumor-profiling assay illustrates how layered genomic, proteomic, and metabolomic data sharpen therapy selection and reduce repeated biopsies. Laboratories justify higher up-front costs through consolidated sampling schedules and improved adherence, supporting the shift toward value-based reimbursement where diagnostic precision demonstrably lowers downstream treatment expense.
Hospitals bought redundant molecular analyzers to cope with pandemic surges; many now run at 40-60% capacity, delaying new capital allocation. Abbott Laboratories disclosed lower 2025 diagnostics revenue as customers exhaust existing stocks instead of upgrading platforms. Price competition grows, compressing margins and elongating replacement cycles by 18-24 months at larger systems.
Other drivers and restraints analyzed in the detailed report include:
For complete list of drivers and restraints, kindly check the Table Of Contents.
Oncology & tumor marker assays are forecast to post a 10.39% CAGR, reflecting pharmaceutical alignment with companion-diagnostic mandates. CBC maintained a 24.24% 2025 clinical diagnostics market share, sustaining base-volume stability in acute and chronic-care pathways.
Expanding multi-parameter oncology panels improve workflow economics by consolidating biomarkers, while lipid profiles face substitution risk from handheld devices that satisfy primary-care turnaround criteria. Infectious-disease menus normalize after pandemic highs yet remain critical in antimicrobial-resistance surveillance programs.
Reagents & kits delivered 64.98% of 2025 revenue, yet data-management software is on track for a 10.62% CAGR as laboratories digitize quality control and regulatory audit trails. Instruments now ship with open APIs that allow middleware to orchestrate sample routing, reagent allocation, and result release in real time, extending asset life amid capital-spending caution. Competitive bidding squeezes reagent margins, prompting vendors to bundle informatics subscriptions that lock in customer loyalty through workflow efficiencies rather than physical consumables.
The Clinical Diagnostics Market Report is Segmented by Test (Lipid Panel, and More), Product (Instruments, Reagents, and More), Technology (Clinical Chemistry, and More), Sample Type (Urine, and More), Setting (Centralized Clinical Laboratories, and More), End User (Hospital Laboratories, Point-Of-Care Settings, and More), and Geography (North America, Europe, and More). The Market Forecasts are Provided in Terms of Value (USD).
North America retained 37.98% 2025 share on high per-capita spending, but Asia-Pacific's 10.14% CAGR underscores widening access and rising chronic-disease incidence. Asia-Pacific is projected to add more than USD 15.62 billion in incremental revenue between 2026 and 2031, buoyed by public-hospital expansion, universal-health-coverage rollouts, and local manufacturing incentives that reduce test cost per capita. Government subsidies encourage decentralized platforms that mitigate specialist shortages in rural districts, allowing the clinical diagnostics market to tap first-time users and drive double-digit unit growth. Multinationals partner with provincial authorities to establish reagent-filling facilities aimed at circumventing import tariffs and shortening lead times.
North America, while mature, remains a technology bellwether. AI-enabled molecular panels and home-specimen logistics have moved from pilot programs to system-wide protocols at integrated-delivery networks. Yet reimbursement constraints and prior-authorization mandates temper volume growth. Laboratories respond by pairing precision oncology tests with real-world-evidence dossiers that justify value under outcome-based contracts. Consolidation persists as regional health systems outsource routine work to large reference labs that optimize scale and invest in next-generation informatics.
Europe faces divergent trajectories: northern countries channel preventive-care budgets into cardiovascular and metabolic-disease screening, whereas southern nations grapple with fiscal austerity that limits adoption of high-priced molecular assays. The European Union's In Vitro Diagnostic Regulation (IVDR) further elevates compliance requirements, prompting smaller manufacturers to exit sub-scale product lines. Still, aging demographics assure steady baseline volume, and cross-border collaborations on rare-disease diagnostics sustain specialized test demand.