
유럽의 암 치료요법 시장은 2025년 614억 6,000만 달러에서 2026년에는 647억 2,000만 달러로 성장하고 2026년부터 2031년에 걸쳐 CAGR 5.31%로 성장을 지속하여 2031년까지 836억 9,000만 달러에 달할 전망입니다.

이 꾸준한 성장 궤도는 유럽 의약품청(EMA)에 의한 규제의 조화, EU 암 대책 계획 하에서의 정밀의료 확대, 독일과 프랑스 등 주요 경제권에서의 지속적인 R&D 투자를 반영하고 있습니다. 경쟁은 항체 약물 복합체(ADC)와 방사성 리간드 요법을 중심으로 전개되는 한편, 바이오시밀러의 도입은 공공 의료 제도 전반적인 비용 억제 노력을 가속화하고 있습니다. 국경을 초월한 CAR-T 제조, 디지털 바이오마커의 도입, 방사성 의약품 스타트업으로의 벤처 캐피탈 급증이 대응 가능한 수요를 더욱 확대하고 있습니다. 하지만 비용 압력, 의료 기술 평가(HTA)의 타임라인 차이, 핵의학 인프라 격차는 환자가 적시에 치료를 받을 수 있게 하는 주요 장벽으로 남아 있습니다.
유럽의약청(EMA)의 근대화로 정밀종양학 승인 과정이 가속화되었고, 2024년에는 28건의 종양학 관련 견해가 발표되었습니다(기존은 연간 한 자릿수). 조건부 판매 승인에 의해 레이저티닙 등의 바이오마커 기반 약제에 대한 시장 투입 기간이 단축되고, 유럽 환자에 대한 제공은 주요 데이터 분석에 따르면 12개월 이내에 실현됩니다. 해당 약물은 대조 요법의 16.6개월에 대해 중앙값 23.7개월의 무진행 생존 기간을 달성했습니다. 현재 실제 임상 데이터(RWE)의 생성을 선호하는 기업은 지속적인 경쟁 우위를 획득하고 있는 한편, 기존 모델에 의존하는 개발 기업은 상시 속도 저하에 직면하고 있습니다. 절차의 조화는 중복 신청을 줄이고 후기 임상시험 및 수명주기 관리에 대한 자본 투입을 유도합니다.
유럽에서의 바이오시밀러의 침투는 트라스투주맙 및 리툭시맙과 같은 부문에서 두 자릿수의 수량 성장을 일으켰고, 주요 시장에서는 가격 하락률을 40% 이상으로 밀어 올렸습니다. 실세계에서의 동등성 연구에 의해 의사의 신뢰가 높아짐으로 도입이 확대되고, 지불 기관은 절약분을 혁신적 치료에 재분배할 수 있게 되었습니다. 선발품 제조업체는 우수한 임상적 차별화와 종합적인 서비스 제공을 강조함으로써 대응하고 있습니다. 여러 공급원에 의한 경쟁이 조달 압력을 강화하고 있으며, 높은 생산 능력 및 생물학적 제제 제조 능력과 견고한 약물 모니터링 데이터 패키지를 가진 제조업체가 우위를 점하고 있습니다.
WAIT(혁신적 치료에 대한 승인 대기 기간) 지표 조사에 따르면, 유럽 5대 시장에서 EMA 승인부터 환자 제공 개시까지의 평균 지연 기간은 531일에 이르며 이는 증거와 가격 요건의 변화를 반영합니다. 2025년 시행된 공동임상평가규제는 조사방법의 통일을 목표로 하지만, 각국기관이 가치평가 틀을 재조정하는 과정에서 이행 마찰이 생겨 격차가 확대될 가능성이 있습니다. 대기업 제약 기업은 다분야에 걸친 시장 접근 팀을 활용하여 병행 신청을 원활하게 진행하고 있지만, 중소 혁신 기업은 출시 연기 및 수익 부족의 위험에 직면하고 있습니다.
2025년 유럽의 암 치료요법 시장 규모에서 화학요법은 41.92%의 점유율을 유지했으며, 이는 병용 요법에서의 확고한 지위를 반영하고 있습니다. 그러나 HER2 음성 유방암 치료요법제의 승인과 무진행 생존 기간을 연장하는 차세대 EGFR 억제제의 등장으로 표적 요법은 6.14%의 연평균 복합 성장률(CAGR)로 확대될 것으로 예측되고 있습니다. 성숙하는 면역요법 기반 치료는 정밀 억제제와의 병용이 증가하고 있어 다양한 종양 유형에서의 효과적인 반응을 가능하게 하고 바이오마커 검사율을 높입니다.
임상시험의 밀도 증가는 종양종에 관계없이 적응증에 대한 전략적 중점화를 뒷받침하고 바구니형 시험 설계가 개발 사이클을 단축하고 있습니다. 전통적인 세포 독성 약물에 대한 바이오시밀러의 침식은 정밀 플랫폼으로의 수익 전환을 가속화하고 기존 제조업체는 라이선싱 및 볼트온 유형 인수에 의한 파이프라인 보충을 요구받고 있습니다. 이 변화는 병원 처방전을 외래 투여로 재지향하고 비용 효과적인 바이오마커 가이드형 프로토콜에 대한 지불자 선호를 강화하고 있습니다.
유방암은 확립된 검진 프로그램과 확립된 치료 알고리즘에 힘입어 2025년 유럽의 암 치료요법 시장의 25.12%를 차지하면서 주도적 지위를 유지하였습니다. 그러나, 제1선택 면역요법인 병용 요법이나 엑손 20 삽입 변이 억제제가 종래의 난치성 영역을 개척하면서, 폐암은 2031년까지 연평균 복합 성장률(CAGR) 6.77%라고 하는 가장 빠른 성장이 전망되고 있습니다.
흡연 규제와 대기질 지표에 대한 환경 정책의 강화는 이환율을 줄일 수 있습니다. 그러나, 분자진단 기술의 급속한 보급으로 가까운 미래에 표적 요법의 대상 환자층은 확대될 전망입니다. 이 때문에 제약기업은 호르몬 수용체 양성 유방암에 대한 블록버스터급 매출 규모와 틈새 폐암 변이에서의 고성장 수익과의 균형을 맞추면서 유전체 서브세트 전체에서의 제품 포트폴리오의 확충을 우선시하고 있습니다.
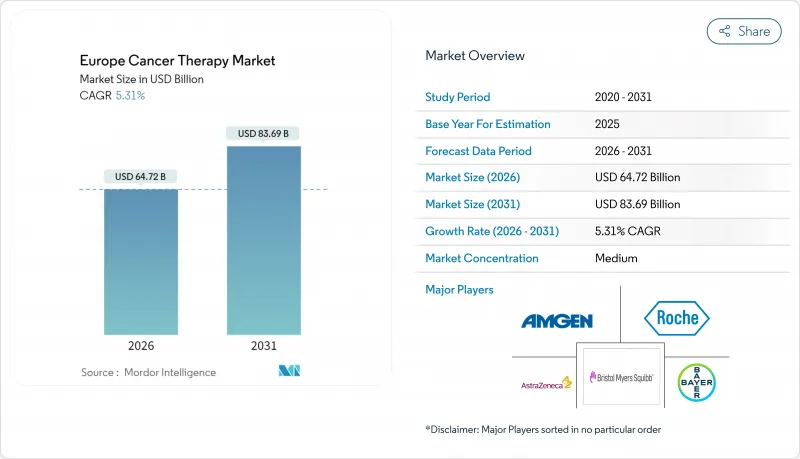
The Europe Cancer Therapy Market is expected to grow from USD 61.46 billion in 2025 to USD 64.72 billion in 2026 and is forecast to reach USD 83.69 billion by 2031 at 5.31% CAGR over 2026-2031.
This steady trajectory reflects regulatory harmonization by the European Medicines Agency (EMA), the expansion of precision medicine under the EU Beating Cancer Plan, and sustained R&D investment in leading economies, such as Germany and France. Intensifying competition centers on antibody-drug conjugates and radioligand therapies, while the uptake of biosimilars accelerates cost containment efforts across public health systems. Cross-border CAR-T manufacturing, digital biomarker deployment, and a surge in venture capital for radiopharmaceutical start-ups further widen the addressable demand. Cost pressures, divergent health-technology assessment (HTA) timelines, and gaps in nuclear-medicine infrastructure remain the principal obstacles to timely patient access.
EMA modernization has accelerated precision-oncology pathways, with 28 oncology opinions in 2024 versus historical single-digit figures. Conditional marketing authorizations shortened time to market for biomarker-driven agents such as lazertinib, which reached European patients within 12 months of pivotal data read-out and delivered 23.7 months median progression-free survival against 16.6 months for comparator therapy. Companies now prioritizing real-world-evidence generation gain a durable competitive edge, whereas developers reliant on legacy models face erosion in launch velocity. Harmonized procedures also reduce duplicative submissions, freeing capital for late-stage trials and life-cycle management.
Europe's biosimilar penetration triggered double-digit volume growth across molecules such as trastuzumab and rituximab, driving price erosion beyond 40% in leading markets. Physician confidence broadened adoption after real-world equivalence studies, enabling payers to reallocate savings to innovative therapies. Originators respond by emphasizing superior clinical differentiation and bundled service offerings. Multi-source competition intensifies procurement pressure, favoring manufacturers with high-throughput biologics capacity and robust pharmacovigilance data packages.
The W.A.I.T. (Waiting to Access Innovative Therapies) indicator survey shows an average 531-day lag between EMA approval and patient availability across the five largest markets, reflecting heterogeneous evidence and pricing requirements. While the 2025 Joint Clinical Assessment regulation aims to align methodologies, transitional frictions may widen gaps as national agencies recalibrate their value frameworks. Larger pharmaceutical firms leverage multi-disciplinary market-access teams to navigate parallel submissions, whereas smaller innovators risk launch postponements and revenue shortfalls.
Other drivers and restraints analyzed in the detailed report include:
For complete list of drivers and restraints, kindly check the Table Of Contents.
Chemotherapy retained a 41.92% share of the Europe cancer therapy market size in 2025, reflecting its entrenched role in combination regimens. Yet targeted therapy is forecast to post a 6.14% CAGR, propelled by HER2-low breast cancer approvals and next-generation EGFR inhibitors that extend progression-free intervals. A maturing immunotherapy backbone is increasingly paired with precision inhibitors, enabling deeper responses across various tumor types and elevating biomarker testing rates.
Increasing clinical trial density underscores a strategic emphasis on tumor-agnostic indications, with basket study designs compressing development cycles. Biosimilar erosion in traditional cytotoxics accelerates revenue migration toward precision platforms, prompting legacy manufacturers to replenish pipelines via licensing or bolt-on acquisitions. The shift also reorients hospital formularies toward outpatient administration, reinforcing payer preference for cost-effective, biomarker-guided protocols.
Breast cancer dominated the Europe cancer therapy market, accounting for a 25.12% share in 2025, driven by established screening programs and well-established treatment algorithms. However, lung cancer is slated for the fastest 6.77% CAGR through 2031 as first-line immunotherapy combinations and exon-20 insertion inhibitors unlock previously refractory segments.
Environmental policy tightening on smoking and air-quality metrics may gradually reduce incidence. Yet, the rapid adoption of molecular diagnostics broadens eligible patient pools for targeted regimens in the near term. Pharmaceutical companies thus prioritize portfolio depth across genomic subsets, balancing blockbuster volume in hormone-positive breast cancer with high-growth revenue in niche lung-cancer mutations.
The Europe Cancer Therapy Market Report is Segmented by Therapy Type (Chemotherapy, Targeted Therapy, and More), Cancer Type (Breast Cancer, Lung Cancer, and More), Drug Class (PD-1/PD-L1 Inhibitors, Tyrosine Kinase Inhibitors, and More), Mode of Administration (Intravenous, Subcutaneous, and More), and Country (Germany, United Kingdom, France, Italy, and More). The Market Forecasts are Provided in Terms of Value (USD).