
세계의 인간 마이크로바이옴 시장 규모는 2025년 10억 5,000만 달러에 이르고, 2030년에는 22억 4,000만 달러에 이를 것으로 예측되며, 기간 중 CAGR은 16.36%로 예상됩니다.
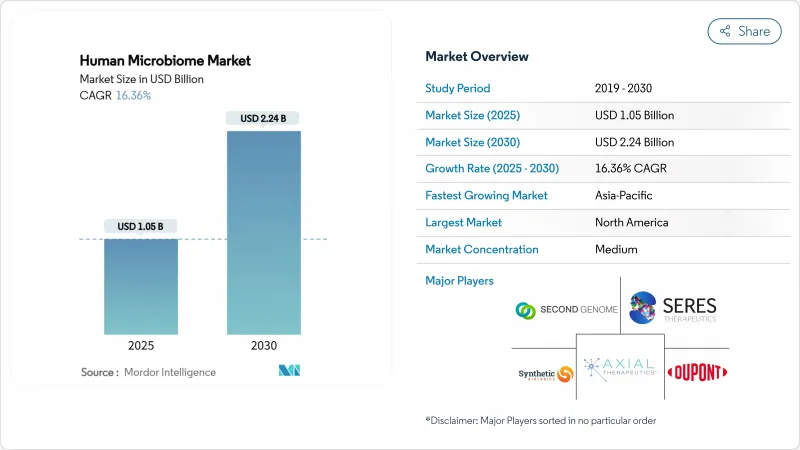
이 확대는 탐구 연구에서 효과적인 치료제로의 결정적인 변화를 반영하고 있으며, FDA에 의한 살아있는 바이오 치료 제품의 승인, 벤처 기업의 자금 조달 가속, 제약 기업의 인수 강화가 박차를 가하고 있습니다. 비용 효율적인 차세대 시퀀싱, 맞춤형 의료에 대한 수요 증가, 장내 미생물과 전신 질환을 연관시키는 임상 증거 증가는 인간 마이크로바이옴 시장의 성장 궤도를 강화하고 있습니다. 업계 참가자들은 또한 복잡한 박테리아 컨소시엄을 상업적 규모로 생산할 수 있는 적절한 제조 기준(GMP) 시설에 대한 규제 지원을 통해 혜택을 누리고 있습니다. 이러한 요인들이 함께 인간 마이크로바이옴 시장은 현대의 의약품 개발·진단의 주류 요소로 자리매김하고 있습니다.
MinION 및 PromethION과 같은 실시간 나노포어 시퀀싱 장치는 샘플당 비용을 약 70% 절감했으며, 한때는 중앙 집중식 실험실이 필요했던 루틴을 프로파일링할 수 있었습니다. 휴대용 플랫폼은 장내 미소 식물상의 포인트 오브 케어 분석을 가능하게 하고 진단의 신속화와 장기적인 모니터링을 지원합니다. PacBio 시스템이 제공하는 전장 16S rRNA 워크플로우는 바이오마커 탐색에 필요한 분류학적 해상도를 더욱 향상시킵니다. 시퀀싱 비용은 100달러대로 추이하고 있으며, 마이크로바이옴 검사를 만성 질환 관리 경로에 통합할 가능성이 높아지고 있습니다. 병원에서는 이미 염증성 장 질환 환자에 대한 정기적인 미생물 감시를 시험적으로 시행하고 있으며, 저렴한 시퀀싱의 임상적 타당성이 확인되었습니다. 이러한 진보가 결합되어 진단 및 치료제 분야에서 인간 마이크로바이옴 시장의 밑단이 확산되고 있습니다.
전문 벤처 펀드와 전략적 기업 투자자들은 2025년 이 분야에 기록적인 자본을 할당하여 유럽, 북미, 동아시아에서 수십 개의 시드 라운드와 시리즈 A 라운드를 홍보했습니다. Aboris Biotechnologies와 같은 유럽 개발 기업은 바이오 제조 능력을 확대하기 위해 3,500만 유로를 확보했으며, CARB-X와 같은 관민 이니셔티브는 항균제 내성 용도를 목표로 한 수백만 달러의 보조금을 교부했습니다. 얀센의 인간 마이크로바이옴 연구소는 신흥 기업이 대규모 의약품 제조업체와 공동 개발할 수 있도록 하는 유연한 파트너십 수단을 수립했습니다. 제약회사와 마이크로바이옴의 제휴에는 미리 정의된 이정표에 연동한 주식 투자가 포함되는 경우가 많아, 젊은 기업에게 자금 조달의 확실성과 멘토에 대한 액세스를 주고 있습니다. 그 결과 자본 유입은 시장 개척의 타임라인을 단축하고, 인재 획득을 촉진하고, 규제 당국에의 신청도 신속화하고, 인간 마이크로바이옴 시장의 상승 모멘텀을 강화합니다.
마이크로바이옴 치료제는 의약품 규제와 이식 규제에 걸쳐 있으며, 크로스보더 임상시험과 시장투입을 늦추는 정책의 모호함을 창출하고 있습니다. FDA, EMA, 일본의 의약품 의료기기 종합기구(PMDA)간에 살아있는 바이오 치료 제품의 정의가 다르기 때문에 신청 서류의 작성이 복잡해져 상호 승인에 대한 의욕이 손상되고 있습니다. 실험실이 DNA 추출, 라이브러리 준비, 바이오인포매틱스 워크플로우를 다양하게 전개하기 때문에 분석상의 불일치가 계속되어 임상의의 신뢰를 저하시키는 일관성 없는 결과가 되고 있습니다. 유럽 연합(EU)의 인간 유래 물질에 관한 규칙은 최종적인 조화를 약속하는 것이지만, 2026년까지는 완전히 발효하지 않습니다. 세계 기준이 통일될 때까지 기업은 지역 특유의 검증 연구에 예산을 나누어야 하며 비용이 상승하고 인간 마이크로바이옴 시장에서의 수익 획득이 지연됩니다.
보충제는 2024년 39.89%의 판매 점유율을 유지했는데, 이는 오랜 소비자 채용과 규제 경로의 간소화를 반영합니다. 한편 의약품은 재발성 클로스트리디움 디피실 감염증에 대한 효과가 임상적으로 증명된 VOWST나 REBYOTA 등의 획기적인 승인에 힘입어 2030년까지 연평균 복합 성장률(CAGR)은 18.21%를 기록할 전망입니다. VOWST의 초기 전개는 2023년 4분기에 1,040만 달러를 벌어 상업적 의욕을 입증하고 추가 신청을 뒷받침했습니다. 프로바이오틱스 보조 식품은 당국이 영양 보조 식품을 살아있는 생물 제제와 구별하기 때문에 제조업체가 무작위 비교 시험에 투자하도록 촉구하고 모니터링을 강화하는 데 직면하고 있습니다.
진단 분석의 기여는 여전히 가장 작지만, 컴패니언 테스트가 종양학 및 대사 시험에서 환자의 층별화에 필수적이 됨에 따라 투자가 활발해지고 있습니다. 포스트 바이오틱스와 인공 세균주는 영양 보충제와 의약품의 가교가 될 수있는 새로운 틈새 분야입니다. 소비자 등급과 처방전 등급 제품의 이분화는 보다 광범위한 인간 마이크로바이옴 시장에서 다양한 수익 흐름을 지원합니다.
2024년 매출액의 69.98%를 치료이용 사례가 차지했지만, 시퀀싱 비용의 급락과 분석 소프트웨어의 성숙에 따라 2030년까지의 예상 CAGR은 진단이 19.12%입니다. 병원 네트워크는 면역 종양 약물에 대한 반응을 예측하는 대변 기반 패널을 시험적으로 도입하여 치료 선택과 상환 결과를 개선합니다. 대변 미생물총 이식은 여전히 전형적인 치료 모델이지만, 파이프라인 자산에는 현재 경구 캡슐, 국소 제형, 대사성 질환, 자가면역 질환, 신경 질환을 표적으로 하는 인공 균주가 포함되어 있습니다.
샘플링 키트, 시퀀싱 서비스, AI 분석 및 표적 개입을 결합한 엔드 투 엔드 플랫폼의 융합은 통합 케어 경로를 약속합니다. 효능이 확인된 진단제를 독자적인 치료제에 묶을 수 있는 시장 개척은 인간 마이크로바이옴 시장 규모 전체에서 매우 큰 가치를 얻을 수 있습니다.
북미는 2024년 세계 매출의 42.28%를 차지하며 FDA 지침, 숙련된 벤처 네트워크, GMP 공장의 임계량에 의해 지원되고 있습니다. 조기 어댑터 병원에서 재발성 클로스트리디움 디피실에 대한 대변 미생물총 이식이 일상적으로 수행되고 종양학의 진단 패널이 시험적으로 도입되었습니다. 보험상환의 명확화는 보다 광범위한 도입을 지원하고 이 지역 시장 역학에 미치는 영향력을 확고히 하고 있습니다.
유럽은 고밀도 학술 클러스터와 협력적인 자금 조달의 틀에서 혜택을 누리고 있습니다. 유럽 위원회의 2025년 생명공학 로드맵은 건강과 지속가능성을 위한 미생물 제제를 우선 과제로 삼고 있습니다. 그러나 각국의 감독체제가 흩어져 있기 때문에 다국간 임상시험은 늦게 진행되지 않고, 제조업체는 고가의 병행신청에 의지하고 있는 것이 현상입니다. 프랑스와 네덜란드와 같은 민간 파트너십은 경쟁력을 유지하기 위한 트랜스레이셔널 자금을 공급하고 있습니다.
아시아태평양은 규제 당국이 통일 규격에 수렴하고 현지 기업이 발효 및 충전 마무리 기능에 자본을 투입하기 때문에 CAGR이 18.65%를 보일 것으로 예측됩니다. 일본에서 2025년에 예정된 JSR-Metagen 공장은 이 지역의 국내 생산 능력 육성에 대한 결의를 예증하고 있습니다. 동남아시아 전역에서 OMNi-BiOTiC 프로바이오틱스를 판매하는 Zuellig Pharma의 10년에 걸친 계약과 같은 파트너십은 대응 가능한 기반을 더욱 확대할 것입니다. 중국과 한국은 마이크로바이옴 프로젝트를 국가의 정밀의료 정책과 결합하여 상업화를 촉진하고 있습니다. 이러한 시장 진출기업들은 인간 마이크로바이옴 시장에 대한 세계적인 진입을 확대하고 있습니다.
The human microbiome market size reached USD 1.05 billion in 2025 and is forecast to climb to USD 2.24 billion by 2030, translating to a 16.36% CAGR during the period.
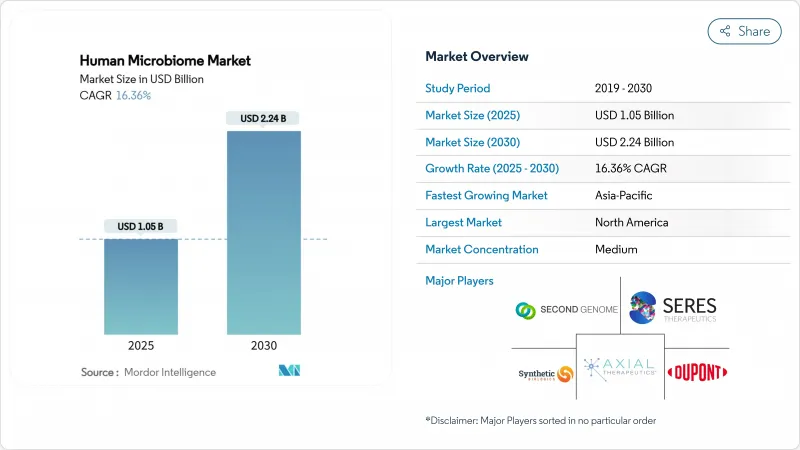
The expansion reflects a decisive shift from exploratory research toward validated therapeutics, spurred by FDA approvals of live biotherapeutic products, accelerating venture funding, and stepped-up pharmaceutical acquisitions. Cost-efficient next-generation sequencing, rising demand for personalized medicine, and growing clinical evidence linking gut microbes to systemic disease are reinforcing the growth trajectory of the human microbiome market. Industry participants are also benefiting from regulatory support for good-manufacturing-practice (GMP) facilities that can produce complex bacterial consortia at commercial scale. Combined, these factors continue to reposition the human microbiome market as a mainstream component of modern drug development and diagnostic practice.
Real-time nanopore sequencing devices such as MinION and PromethION have cut per-sample costs by roughly 70%, enabling routine profiling that once required centralized laboratories . Portable platforms permit point-of-care analysis of gut microflora, accelerating diagnostic turnaround and supporting longitudinal monitoring. Full-length 16S rRNA workflows delivered by PacBio systems further increase taxonomic resolution needed for biomarker discovery. Sequencing expenditures are trending toward the USD 100 threshold, elevating the feasibility of incorporating microbiome checks into chronic-disease management pathways . Hospitals are already piloting regular microbial surveillance for inflammatory bowel disease patients, confirming the clinical relevance of affordable sequencing. Combined, these advances are widening the addressable base of the human microbiome market across both diagnostics and therapeutics.
Dedicated venture funds and strategic corporate investors allotted record capital to the sector in 2025, catalyzing dozens of seed and Series A rounds in Europe, North America, and East Asia. European developers such as Abolis Biotechnologies secured EUR 35 million to scale biomanufacturing capacity, while public-private initiatives like CARB-X handed out multimillion-dollar grants targeting antimicrobial-resistance applications. Janssen's Human Microbiome Institute cemented flexible partnership vehicles that enable start-ups to co-develop co-therapy assets with large-scale drug manufacturers . Pharma-microbiome alliances frequently include equity investments tied to predefined milestones, giving young companies funding certainty and mentor access. The resultant capital inflows shorten development timelines, drive talent acquisition, and speed regulatory submissions, reinforcing the upward momentum of the human microbiome market.
Microbiome therapeutics straddle medicinal-product and transplant regulations, generating policy ambiguity that slows cross-border trials and market launches. Divergent definitions of live biotherapeutic products across the FDA, EMA, and Japan's PMDA complicate dossier preparation and compromise mutual-recognition ambitions. Analytical discord persists as laboratories deploy varied DNA-extraction, library-prep, and bioinformatics workflows, producing inconsistent readouts that dampen clinician trust. Upcoming European Union rules governing substances of human origin promise eventual harmonization but will not take full effect before 2026. Until global norms converge, companies must budget for region-specific validation studies, raising costs and delaying revenue capture in the human microbiome market.
Other drivers and restraints analyzed in the detailed report include:
For complete list of drivers and restraints, kindly check the Table Of Contents.
Supplements maintained a 39.89% revenue share in 2024, reflecting longstanding consumer adoption and streamlined regulatory routes. Drugs, however, are on track to register an 18.21% CAGR through 2030, buoyed by landmark approvals such as VOWST and REBYOTA, which showcase clinically proven benefits against recurrent C. difficile infections. Initial roll-out of VOWST generated USD 10.4 million in Q4 2023, validating commercial appetite and emboldening additional filings. Probiotic supplements face mounting scrutiny as authorities delineate dietary products from live biotherapeutic drugs, prompting manufacturers to invest in randomized controlled trials.
Diagnostic assays remain the smallest contributor but attract intensified investment as companion tests become essential for patient stratification in oncology and metabolic trials. Postbiotics and engineered bacterial strains represent emerging niches that may bridge nutraceutical and pharmaceutical spaces. The bifurcation of consumer-grade and prescription-grade offerings underpins diversified revenue streams within the broader human microbiome market.
Therapeutic use cases accounted for 69.98% of revenue in 2024, yet diagnostics enjoy a forecast 19.12% CAGR to 2030 as sequencing costs plummet and analytical software matures. Hospital networks are piloting stool-based panels that predict response to immuno-oncology agents, improving treatment selection and reimbursement outcomes. Fecal microbiota transplantation remains the archetypal therapeutic model, but pipeline assets now encompass oral capsules, topical formulations, and engineered strains targeting metabolic, autoimmune, and neurologic diseases.
The convergence of end-to-end platforms that combine sampling kits, sequencing services, AI analytics, and targeted interventions promises integrated care pathways. Developers able to link a validated diagnostic to a proprietary therapeutic could capture outsized value across the human microbiome market size.
The Human Microbiome Market Report is Segmented by Product (Drugs, Supplements, Diagnostic Tests, Other Products), Application (Therapeutics, Diagnostics), Disease Area (Gastrointestinal Disorder, Cancer, and More), End-User (Hospitals and Clinics, and More), and Geography (North America, Europe, Asia-Pacific, Middle East and Africa, South America). Market Forecasts are Provided in Terms of Value (USD).
North America commanded 42.28% of global revenue in 2024, underpinned by FDA guidance, seasoned venture networks, and a critical mass of GMP plants. Early adopter hospitals routinely implement fecal microbiota transplantation for recurrent C. difficile and are piloting diagnostic panels for oncology. Increasing reimbursement clarity supports broader uptake, solidifying the region's influence on human microbiome market dynamics.
Europe benefits from dense academic clusters and coordinated funding frameworks; the European Commission's 2025 biotechnology roadmap prioritizes microbial therapeutics for health and sustainability. Yet divergent national oversight regimes slow multicountry trials, keeping manufacturers reliant on expensive parallel submissions. Public-private partnerships such as those in France and the Netherlands supply translational funding that sustains competitiveness.
Asia-Pacific is projected to record an 18.65% CAGR as regulators converge on harmonized standards and local companies pour capital into fermentation and fill-finish capabilities. The JSR-Metagen plant scheduled for 2025 in Japan exemplifies the region's resolve to nurture domestic production capacity. Partnerships like Zuellig Pharma's decade-long deal to distribute OMNi-BiOTiC probiotics across Southeast Asia further enlarge the addressable base. China and South Korea expedite commercialization by bundling microbiome projects with national precision-medicine policies. Collectively, these developments broaden global participation in the human microbiome market.