
세계의 단백질 공학 시장 규모는 2025년에 40억 9,000만 달러로 추정되고, 2030년에는 86억 8,000만 달러에 이를 것으로 예측되며, CAGR 16.24%로 성장이 전망됩니다.

이러한 강력한 확장은 기존의 시행착오 기법에서 AI를 활용한 설계 플랫폼으로의 결정적인 전환, 생물제제 규제 경로의 신속화, 공적 자금의 지속적인 투입을 반영합니다. 구글 딥 마인드의 AlphaProteo 시스템으로 대표되는 인실리코 모델링의 급속한 진보는 결합 친화성을 기존 기술의 300배까지 향상시키고, 개발 사이클을 단축하며, 치료제의 대응 가능한 기회를 넓히고 있습니다. 만성 질환의 유행, 예방 및 치료용 백신에 있어서 mRNA 기술의 성공, 다액의 자본을 필요로 하지 않고 전문 지식을 제공할 수 있는 연구 수탁 기관에 대한 아웃소싱의 확대도, 수요의 춘풍이 되고 있습니다. 기존 장비 공급업체가 디지털 기능을 강화하는 한편, AI 네이티브 신흥기업이 대규모 벤처 자금과 10억 달러 규모의 제휴를 맺어 진입하는 등 경쟁 역학은 변화하고 있으며, 생태계는 유동적이면서 제휴 기회가 풍부하다는 것을 보여주고 있습니다.
단일클론항체는 계속 후기 단계의 파이프라인을 선도하고 있으며, FDA 승인의 가속과 암 영역 이외의 적응 확대에 의해 2025년에는 연간 3,150억 달러의 매출이 될 것으로 예측되고 있습니다. 현재 신규 신청에서는 이중특이성 제제가 주목할만한 점유율을 차지하고 있으며, RSV 예방을 위한 머크 크레스로비맙 등 최근 승인은 치료법의 폭넓은 점을 뒷받침하고 있습니다. 제조 기술 혁신은 Sutro Biopharma의 항체 약물 복합체의 상업적 규모의 무 세포 발현으로 대표되는 제품 비용을 낮추고 있습니다. 이러한 결과는 환자 접근을 개선하고 단백질 공학 시장의 수익 기반을 강화합니다.
인공지능으로 인해 약물의 타임라인은 수년에서 수개월로 단축되고 있습니다. AlphaProteo는 기존 기술에 비해 300배의 친화성 향상을 보여줍니다. Generate : Biomedicines사의 Chrome은 310개의 실험적으로 검증된 단백질을 유리한 특성으로 검증하였으며, 노바티스사와 10억 달러의 멀티타겟 계약을 지원했습니다. 뮌헨 공과 대학의 연구자들은 AlphaFold2를 1,000개의 아미노산 설계로 확장하여 예측과 맞춤형 서열 생성의 격차를 메웠습니다. 이러한 발전으로 AI는 단백질 공학 시장의 주요 성장 엔진으로 자리매김하고 있습니다.
세련된 장비, 단일 셀 단백질체학 워크플로우, 독자적인 시약은 자본 집약도를 높게 유지하고 있습니다. 단일 셀의 단백질 분석은 처리량에 따라 세포당 2달러 이하에서 50달러 이상이 될 수 있습니다. 업계의 시산에서는 신규 단백질을 스케일 업하기 위해서는 수십억 달러의 투자가 필요하다고 지적되고 있으며, 이러한 부담은 중소기업에서는 아웃소싱이나 시설의 공유에 의해 경감되는 경우가 많습니다. 로봇을 활용한 저비용 효소 탐색 파이프라인은 귀찮은 작업을 자동화하여 비용 격차를 줄이기 시작했습니다. 이러한 기술 혁신이 압력을 완화하는 한편, 고액의 선행 투자는 여전히 단백질 공학 시장을 완화하는 힘이 되고 있습니다.
단일클론항체는 2024년 매출의 40.35%를 차지하였고, 단백질 공학 시장에서 가장 큰 슬라이스를 확보했습니다. 지속적인 규제 당국의 승인, 적응증의 확대, 무세포 발현과 같은 제조의 진보에 의해 진입 장벽은 높게 유지되는 한편, 상업적 예측 가능성은 확고해집니다. 백신은 2030년까지 연평균 복합 성장률(CAGR) 18.25%를 기록할 전망이며, mRNA의 범용성을 활용하여 신속한 항원 설계와 견고한 면역원성을 실현합니다. 이중특이성 및 항체 약물 복합체에 대한 지속적인 투자는 이 부문의 파이프라인의 강인성을 더욱 강화합니다.
백신의 기회는 팬데믹 대책비로부터 기세를 늘리고, AI에 의한 항원 설계가 후보품 선정을 가속하고 있습니다. 인슐린과 응고 인자는 성숙한 상태이지만, 장시간 작용형 제제나 유전자 치료의 대체품을 통해 진화하고 있습니다. 성장 인자와 융합 단백질은 재생 의학 및 대사성 질환의 틈새에 대응하고 품질 모니터링을 개선하는 FDA의 신속한 당쇄 프로파일링 방법과 같은 규제 이니셔티브에 의해 지원됩니다. 이러한 개발은 단백질 공학 시장의 확대 기조를 뒷받침하고 있습니다.
소모품은 2024년 매출의 52.53%를 차지했으며, 실험실 워크플로우 전반에 걸쳐 시약 및 키트에 대한 수요가 반복됨을 뒷받침하고 있습니다. 그러나 소프트웨어 및 서비스는 CAGR 19.85%에서 가장 급속히 확대될 것으로 예측되며, 이는 AI를 활용한 모델링과 클라우드 기반 협업에 업계가 축족을 두고 있음을 보여줍니다. 소프트웨어 및 서비스의 단백질 공학 시장 규모는 알고리즘이 총 스크리닝을 대체할수록 하드웨어 예산을 초과할 것으로 예측됩니다.
컴퓨터를 이용한 접근은 소규모 기업의 진입 장벽을 낮춥니다. Generate : Biomedicines의 Novartis와 10억 달러 규모의 제휴와 Cradle의 7,300만 달러 시리즈 B는 알고리즘 설계가 창약 기간을 단축할 수 있다는 자신감을 반영합니다. 차세대 단백질체학를 심화시키는 서모 피셔사의 Olink사 인수(31억 달러)로 분석 장치는 꾸준히 업그레이드되고 있습니다. 하드웨어가 디지털 플랫폼과 통합됨에 따라 시너지 효과가 단백질 엔지니어링 시장의 다음 효율성 도약의 원동력이 될 것입니다.
북미는 미국의 성숙한 벤처 에코시스템, 일류의 학술 연구, 혁신에 보상하는 FDA 정책에 힘입어 2024년 매출 공헌률 44.82%로 단백질 공학 시장을 선도했습니다. DARPA의 Switch 이니셔티브와 NSF의 4,000만 달러의 단백질 설계 보조금 풀과 같은 연방 프로그램은 이 지역의 이점을 증폭시키고 있습니다. 엘라이 릴리와 노보놀 디스크는 GLP-1 생산을 지원하는 노스캐롤라이나의 새로운 시설에 61억 달러를 투자하고 있습니다. 단백질 공학 시장은 창약 연구소, 규제 당국 및 확장 가능한 생산 능력 사이의 근접성으로 이익을 얻고 있습니다.
아시아태평양의 CAGR은 19.61%로 2030년까지 이 지역에서 가장 빠른 성장이 예측되고 있습니다. 중국은 자본 시장의 역풍에도 불구하고 바이오테크놀러지 자급에 대한 헌신으로 2024년 기업 자금으로 4억 7,100만 달러를 차지했습니다. 한국은 발효 전문 지식을 농업 혁신과 결합하고 있으며 호주 CSIRO는 최근 4,450만 달러의 보조금으로 2040년까지 300억 달러의 합성 생물학 산업을 예측했습니다. 일본 에코시스템은 가격 압력으로 지연을 겪고 있지만, 중외 제약과 같은 국내 챔피언은 독자적인 항체 기술을 강점으로 2024년에 기록적인 매출을 달성했습니다. 이러한 개발로 단백질 공학 시장에서 아시아태평양의 지위가 한층 높아지고 있습니다.
유럽은 협조적인 정책과 강력한 학술 네트워크에 힘입어 여전히 영향력 있는 노드로 남아 있습니다. EU의 2024년 '자연과 함께 미래 구축' 청사진은 생명공학의 주권과 지속가능성을 추진하고 있습니다. 영국의 1억 파운드(1억 2,500만 달러)의 공학 및 생물학 프로그램은 팬데믹에 대한 대비를 가속화하고 있으며, 뉴클레라의 114만 파운드(140만 달러)의 Innovate UK 보조금은 신속한 단백질 발현 도구를 위한 시드 스테이지 지원을 보여줍니다. 네덜란드의 6,000만 유로(6,500만 달러)의 세포 배양 펀드는 생명공학 원칙을 식품 시스템으로 확대하는 것입니다. 이러한 이니셔티브는 유럽의 경쟁력을 유지하고 단백질 공학 시장의 세계적인 발자국을 다양화하는 것입니다.
The global protein engineering market is currently valued at USD 4.09 billion in 2025 and is forecast to climb to USD 8.68 billion by 2030, translating into a 16.24% CAGR.
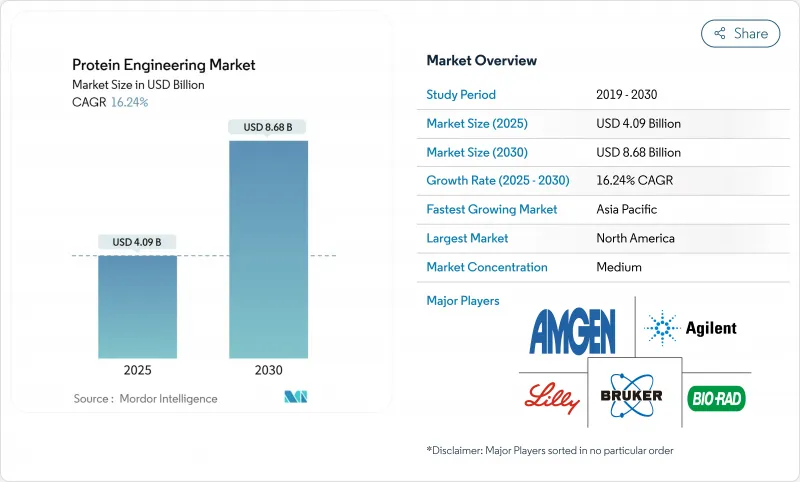
This strong expansion reflects a decisive move away from traditional trial-and-error methods toward AI-enabled design platforms, faster regulatory pathways for biologics, and sustained public-sector funding. Rapid advances in in-silico modeling, exemplified by Google DeepMind's AlphaProteo system that delivers binding affinities up to 300-fold better than earlier techniques, are compressing development cycles and widening the addressable opportunity for therapeutics. Demand also benefits from chronic-disease prevalence, the success of mRNA technology in prophylactic and therapeutic vaccines, and growing outsourcing to contract research organizations that can provide specialized expertise without heavy capital requirements. Competitive dynamics are shifting as incumbent instrument suppliers strengthen digital capabilities while AI-native startups enter with significant venture funding and billion-dollar collaborations, signalling an ecosystem in flux yet rich in partnership opportunities.
Monoclonal antibodies continue to headline late-stage pipelines, with forecasts pointing to USD 315 billion in annual sales by 2025, propelled by accelerated FDA approvals and expanded indications beyond oncology. Bispecific formats now comprise a notable share of new filings, and recent clearances such as Merck's clesrovimab for RSV prevention underscore the therapeutic breadth. Manufacturing innovation is lowering cost-of-goods, exemplified by Sutro Biopharma's commercial-scale cell-free expression of an antibody-drug conjugate. These gains improve patient access and reinforce the revenue base for the protein engineering market.
Artificial intelligence is compressing discovery timelines from years to months. AlphaProteo has shown 300-fold affinity improvements over legacy techniques. Generate:Biomedicines' Chroma validated 310 experimentally tested proteins with favorable properties, underpinning a USD 1 billion multi-target deal with Novartis. Technical University of Munich researchers extended AlphaFold2 to 1,000-amino-acid designs, bridging a gap between prediction and custom sequence generation. Collective advances position AI as a primary engine of growth for the protein engineering market.
Sophisticated equipment, single-cell proteomics workflows and proprietary reagents keep capital intensity high. Single-cell protein analysis can range from under USD 2 to more than USD 50 per cell depending on throughput. Industry estimates point to multibillion-dollar investment needs to bring novel proteins to scale, a burden that smaller firms often mitigate by outsourcing or sharing facilities. Robotics-enabled, low-cost enzyme discovery pipelines are beginning to narrow cost gaps by automating tedious tasks. While these innovations ease pressure, high upfront spending remains a moderating force on the protein engineering market.
Other drivers and restraints analyzed in the detailed report include:
For complete list of drivers and restraints, kindly check the Table Of Contents.
Monoclonal antibodies retained 40.35% of 2024 revenue, securing the largest slice of the protein engineering market. Sustained regulatory approvals, broadening indications and manufacturing advances such as cell-free expression keep entry barriers high while cementing commercial predictability. Vaccines are set to register an 18.25% CAGR through 2030, leveraging mRNA versatility to deliver rapid antigen design and robust immunogenicity. Continued investment in bispecifics and antibody-drug conjugates further fortifies the segment's pipeline resilience.
The vaccine opportunity gains momentum from pandemic preparedness spending, with AI-directed antigen design accelerating candidate selection. Insulin and coagulation factors remain mature but evolve through long-acting formulations and gene-therapy alternatives. Growth factors and fusion proteins address regenerative medicine and metabolic disease niches, supported by regulatory initiatives such as the FDA's rapid glycan-profiling method that improves quality oversight. Collectively, these developments reinforce the expansion trajectory of the protein engineering market.
Consumables generated 52.53% of 2024 revenue, underscoring the recurring demand for reagents and kits across laboratory workflows. Yet software and services are projected to scale fastest at a 19.85% CAGR, signifying an industry pivot toward AI-enabled modeling and cloud-based collaboration. The protein engineering market size for software and services is expected to outpace hardware budgets as algorithms replace brute-force screening.
Compute-rich approaches lower the barrier for smaller entities to participate. Generate:Biomedicines' billion-dollar alliance with Novartis and Cradle's USD 73 million Series B reflect confidence that algorithmic design can shorten discovery timelines. Instruments still see steady upgrades, highlighted by Thermo Fisher's USD 3.1 billion Olink acquisition that deepens next-generation proteomics. As hardware integrates with digital platforms, synergy will drive the next efficiency leap within the protein engineering market.
The Protein Engineering Market Report is Segmented by Protein Type (Insulin, Monoclonal Antibodies, Vaccines, and More), Product & Service (Instruments, Consumables, and Software & Services), Technology (Irrational Design, Rational Design, and Hybrid Design), End User (Pharmaceutical and Biotechnology Companies, and More), and Geography (North America, Europe, and More). The Market Forecasts are Provided in Terms of Value (USD).
North America led the protein engineering market with a 44.82% revenue contribution in 2024, anchored by the United States' mature venture ecosystem, premier academic research and FDA policies that reward innovation. Federal programs such as DARPA's Switch initiative and the NSF's USD 40 million protein-design grant pool amplify the regional advantage. Biopharma manufacturers are reinforcing supply chains through large domestic builds; Eli Lilly and Novo Nordisk together earmarked USD 6.1 billion for new facilities in North Carolina that will support GLP-1 production. The protein engineering market benefits from proximity between discovery labs, regulators and scalable production capacity.
Asia-Pacific is forecast to grow at 19.61% CAGR, the fastest regional clip through 2030. China's commitment to biotech self-sufficiency yielded USD 471 million in 2024 start-up funding despite capital-market headwinds. South Korea is pairing fermentation expertise with agricultural innovation, while Australia's CSIRO projects a USD 30 billion synthetic-biology industry by 2040 supported by USD 44.5 million in recent grants. Japan's ecosystem lags due to pricing pressures, yet domestic champions such as Chugai delivered record 2024 revenue on the strength of proprietary antibody technologies. These developments collectively sharpen Asia-Pacific's stake in the protein engineering market.
Europe remains an influential node, supported by coordinated policy and a strong academic network. The EU's 2024 "Building the Future with Nature" blueprint promotes biotechnology sovereignty and sustainability. The United Kingdom's GBP 100 million (USD 125 million) engineering-biology program accelerates pandemic readiness, while Nuclera's GBP 1.14 million (USD 1.4 million) Innovate UK grant exemplifies seed-stage support for rapid protein expression tools. The Netherlands' EUR 60 million (USD 65 million) cellular-agriculture fund extends biotech principles into food systems. These initiatives maintain Europe's competitiveness and diversify the global footprint of the protein engineering market.