
항체약물접합체(ADC) 시장 규모는 2026년에는 200억 9,000만 달러로 추정되고 있으며, 2025년 156억 1,000만 달러에서 성장을 이룹니다.
2031년의 예측에서는 709억 1,000만 달러에 달하며, 2026-2031년에 CAGR 28.68%로 확대할 전망입니다.
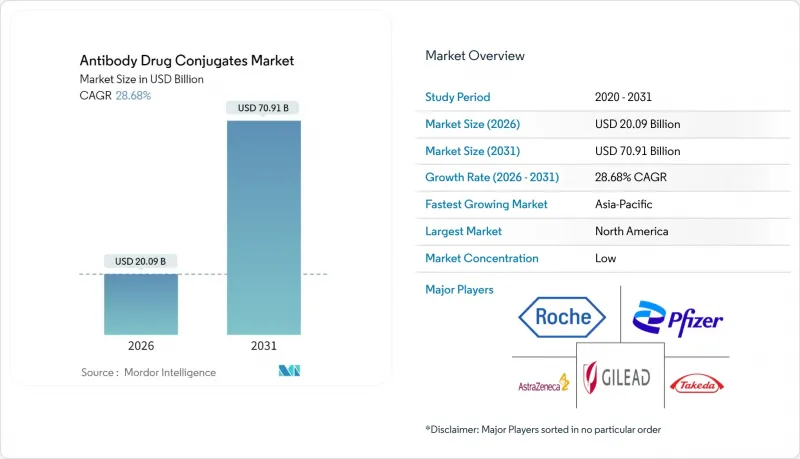
이러한 확대는 항체-약물 접합체 산업 전반에 걸쳐 강력한 세포독성 물질을 악성 세포에 직접 전달하여 전신 독성을 억제하는 정밀 종양학으로의 명확한 전환을 반영하고 있습니다. 투자자들은 ADC의 치료 지수 향상을 자본 배분의 촉매제로 자주 언급하고 있습니다. 이러한 추세는 초기 개발 단계의 자금 조달에 필요한 위험 허용치를 분명히 낮추고 있습니다. 또한 병원에서는 다일간의 입원 화학요법 대신 당일 정맥주사 치료로 대응하기 위해 암 치료 경로의 재구축을 지속하고 있다는 점도 시사하는 바가 큽니다. 이러한 워크플로우의 변화는 병상 점유 기간 단축과 간접적인 병원 영업 이익률 향상으로 이어져 ADC 도입의 매력을 더욱 높이고 있습니다.
이러한 임상적, 재무적 우위와 함께 경쟁 환경의 통합도 가속화되고 있습니다. 화이자의 430억 달러 규모의 시젠 인수는 링커 케미컬, 고효능 페이로드, 상업적 규모를 아우르는 통합 플랫폼을 제공합니다. 업스트림 공정에서는 제일약품이 상하이에 1억 5,200만 달러를 투자하여 고활성 물질 제조공장을 건설 중에 있으며, 중국에서의 상환 범위 확대에 따라 엔헤르츠의 안정적 공급을 확보할 수 있습니다. 미국 식품의약국(FDA)은 2024년 3월 ADC 전용 임상약리학 가이던스를 발표하고, 약물상호작용비(DAR)의 일관성에 대한 품질 기준을 상향 조정하는 등 규제 당국의 요구사항도 강화되고 있습니다.
과거 혈액암에 국한되었던 반응률에 힘입어 고형암은 신규 ADC 임상시험에서 가장 큰 비중을 차지하게 되었습니다. HER2 변이 비소세포폐암 후보물질의 초기 단계 데이터에서 38% 이상의 전체 반응률을 보이며, 이 약물의 범용성을 입증했습니다. 이러한 효과로 인해 임상의들은 특히 오랜 기간 중 약제 내성을 보인 종양에서 기존의 화학요법 기반을 재평가해야 하는 상황에 직면해 있습니다. 최근 수탁제조업체는 고형종양 미세환경에 최적화된 절단형 링커의 주문이 장기화되고 있다고 보고하고 있으며, 향후 생산 규모 확대를 시사하고 있습니다.
고령화로 인해 강력한 세포독성 약물을 견디지 못하는 암 환자층이 확대되면서 외래 치료에 적합한 안전성 프로파일을 가진 ADC에 대한 수요가 증가하고 있습니다. 관찰 연구에 따르면 체지방 분포가 트러스트주맙 델크스테칸의 체중 감소에 영향을 미치는 것으로 나타나 임상의들이 고령자를 위한 치료법을 개별화하려는 움직임이 가속화되고 있습니다. 영상 진단센터에서는 현재 일상적인 병기 분류에 체성분 분석을 통합하고 있으며, 이를 통해 진단 매출이 조금씩 증가하고 있습니다. 지불 기관은 ADC를 입원 비용을 상쇄하는 수단으로 인식하는 경향이 강해졌고, 이는 보다 유리한 상환 결정으로 이어지고 있습니다.
오리스타틴 및 PBD 페이로드공급 제약은 계속되고 있으며, 그 주요 요인은 고활성 성분의 복잡한 봉쇄 요건에 기인합니다. 싱가포르와 상하이에 건설된 수십억 달러 규모의 새로운 시설은 기업이 출시 일정을 지키기 위해 생산을 내재화하고 있음을 보여줍니다. 이러한 프로젝트에도 불구하고 조달팀은 여전히 덜 까다로운 대체 페이로드 클래스를 찾아 위험을 헤지하기 위해 노력하고 있습니다. 이러한 노력은 간접적으로 다양한 화학기지에 대응할 수 있는 차세대 링커에 대한 수요를 증가시켜 점진적인 공정 혁신을 촉진하고 있습니다.
엔하르트는 2025년 항체약물접합체(ADC) 시장에서 22.80%의 점유율을 차지할 것으로 예상되며, 2031년까지 30.17%의 연평균 복합 성장률(CAGR)로 선두를 유지할 것으로 예측됩니다. 이러한 모멘텀은 유방암, 위암, 폐암 등 다양한 적응증에 대한 승인으로 여러 적응증에 걸쳐 수입원을 창출하고 있기 때문입니다. 기존 1차 HER2 치료제의 우월성을 입증하는 임상적 증거로 인해 보험사들은 1차 치료제의 보험 적용 범위 확대에 대한 압력이 커질 수 있습니다.
애드세트리스는 혈액학 영역에서 그 중요성을 유지하고 있지만, 대세포 B세포 림프종에 대한 적응증 확대는 새로운 성장 가능성을 시사하고 있습니다. 요로상피암에 대한 파도세브와 펨브롤리주맙 병용요법은 사망 위험을 거의 절반으로 감소시켜 지역 의료현장에서의 채택을 촉진하고 있습니다. 사시투주맙-틸모테칸과 같은 신규 개발품은 난치성 질환에서 차별화를 제공하기 위해 이중 페이로드 구성에 중점을 둔 파이프라인을 강조하고 있습니다. 이들 제품군은 종합적으로 항체약물접합체(ADC) 시장 규모가 적응증의 폭과 특정 암종에 대한 깊이 있는 데이터로 인해 혜택을 받고 있음을 보여줍니다.
2025년 기준 절단 가능한 링커가 항체약물접합체 시장 규모의 약 69.20%를 차지했으며, 부위 특이적 결합 기술은 2031년까지 30.08% 이상의 CAGR로 성장할 것으로 예측됩니다. 세포 외 절단형 설계는 전신 안정성을 높이면서 확실한 세포내 방출을 보장하는 특성을 가지고 있으며, 규제 당국에서도 높이 평가하고 있는 조합입니다.
효소 코드 확장법 또는 유전자코드 확장법을 이용한 부위 특이적 플랫폼은 균일한 약물 항체 비율(DAR)을 실현하여 임상 투여량을 줄일 수 있습니다. 이러한 추세는 제조 분석이 고처리량 DAR 확인 분석으로 전환되고 있음을 시사하며, 전문 CRO(Contract Research Organization)에 새로운 비즈니스 기회를 창출할 수 있습니다. 비절단성 링커는 점유율이 줄어들고 있지만, 조기 단절에 취약한 페이로드 용도에서 여전히 선호되고 있으며, 틈새 수요가 지속될 것으로 보입니다.
북미는 2025년 기준 전 세계 항체약물접합체(ADC) 시장 규모의 41.20%를 차지할 것으로 예측됩니다. 이는 FDA의 조기 승인과 집중적인 연구 인프라가 지원된 결과입니다. 의사의 바이오마커 검사에 대한 숙련도가 높기 때문에 환자를 빠르게 식별할 수 있으며, 도입 지연을 압축하는 요인으로 작용하고 있습니다. 이 지역의 상환 프레임워크에는 현재 ADC 전용 지불 코드가 포함되어 있으며, 신규 출시 제품의 매출 인식 주기를 단축하고 있습니다. 미국의 암 치료 네트워크는 원격의료를 통합하고 관리 가능한 독성에 대한 후속 진료가 가상 플랫폼으로 이동하여 클리닉의 용량을 확보할 수 있게 되었습니다.
아시아태평양은 암 발병률 증가와 지원적인 국가 보험 정책에 힘입어 2031년까지 31.43% 이상의 예측 CAGR로 가장 빠르게 성장하는 지역입니다. 중국이 ADC를 급여 리스트에 추가하면서 처방량이 눈에 띄게 증가하여 정책이 보급을 이끄는 실례를 보여주고 있습니다. 현지 기업이 세계 임상시험에 참여하기 시작하면서 향후 수출에 대한 의지가 엿보입니다. 일본의 외래진료 수가 개혁은 당일 입원 치료를 촉진하여 병원 경영을 지원하고 있습니다. 유력한 파급효과로 고효능 페이로드를 전문으로 하는 지역 수탁제조 기업이 다국적 기업과의 제휴를 유치하여 아시아태평양의 제조 경쟁력을 강화할 것으로 예측됩니다.
유럽은 엄격한 의료 기술 평가 과정과 전문 치료 센터를 배경으로 항체약물접합체 시장에서 여전히 중요한 점유율을 유지하고 있습니다. 독일의 외래진료 수가체계 개편은 병원의 비용절감으로 이어져 조용히 지역 경쟁력을 높이고 있습니다. 영국의 암치료제 기금은 본격적인 평가가 진행되는 동안에도 잠정적인 접근을 허용하는 경우가 많아 환자들의 대기 시간을 단축하고 있습니다. 중동 및 남미 시장은 규모는 작지만, 3차 의료시설에서 조기 도입 추세를 보이고 있으며, 향후 성장 가능성을 보여주고 있습니다. 이들 지역에서는 예산에 미치는 영향을 완화하기 위해 관리형 도입 계약을 도입할 가능성이 있으며, 가치 기반 가격 책정 시범 사업을 위한 비옥한 토양이 조성되고 있습니다.
Antibody Drug Conjugate market size in 2026 is estimated at USD 20.09 billion, growing from 2025 value of USD 15.61 billion with 2031 projections showing USD 70.91 billion, growing at 28.68% CAGR over 2026-2031.
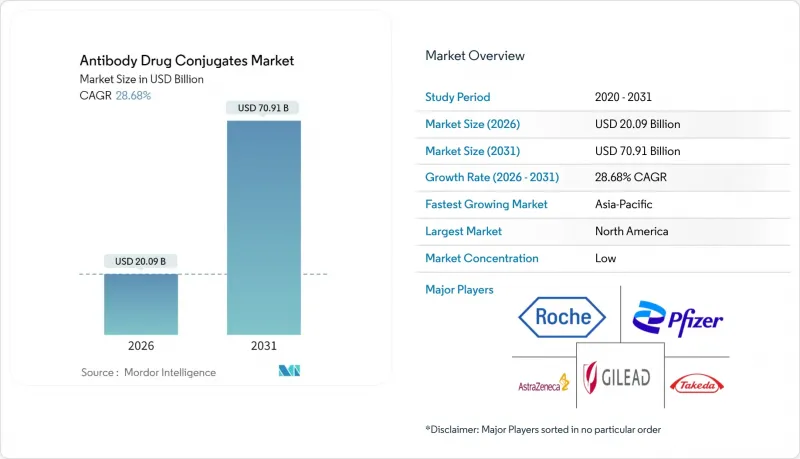
This expansion mirrors a clear shift within the broader Antibody Drug Conjugate industry toward precision oncology, where the capacity to deliver potent cytotoxins directly to malignant cells limits systemic toxicity. Investors frequently cite the improved therapeutic index of ADCs as a catalyst for capital allocation, a trend that is visibly lowering the risk appetite required to fund early-stage development. A further implication is that hospitals continue to reengineer oncology pathways to accommodate day-care infusions rather than multi-day inpatient chemotherapy regimens. These workflow changes appear to shorten bed occupancy and indirectly improve hospital operating margins, reinforcing the attractiveness of ADC adoption.
Parallel to those clinical and financial advantages, competitive consolidation is gathering speed. Pfizer's USD 43 billion acquisition of Seagen provides an integrated platform covering linker chemistry, potent payloads, and commercial scale. Upstream, Daiichi Sankyo is building a USD 152 million high-potency plant in Shanghai to ensure uninterrupted Enhertu supply as Chinese reimbursement expands. Regulatory agencies are also sharpening expectations: the United States Food and Drug Administration released stand-alone clinical-pharmacology guidance for ADCs in March 2024, raising quality benchmarks on drug-to-antibody ratio (DAR) consistency.
Solid tumors increasingly account for the largest share of new ADC trials, propelled by response rates once limited to blood cancers. Early-phase data for a HER2-mutant non-small cell lung cancer candidate demonstrated an overall response rate north of 38%, underscoring class versatility . That efficacy is spurring clinicians to re-evaluate entrenched chemotherapy backbones, especially in tumors with long-standing drug resistance. An immediate outcome is that contract manufacturers report longer order books for cleavable linkers optimized for solid-tumor microenvironments, hinting at forthcoming production scale-ups.
Demographic aging is swelling the pool of oncology patients who cannot tolerate intensive cytotoxics, elevating demand for ADCs with outpatient-friendly safety profiles. Observational evidence shows body-fat distribution influences dose reductions for trastuzumab deruxtecan, prompting clinicians to personalize regimens for older adults. Imaging centers now integrate body-composition analytics into routine staging, subtly raising diagnostic revenues . Payers increasingly view ADCs as tools to offset downstream hospitalization costs, leading to more favorable reimbursement decisions.
Auristatin and PBD payloads remain in constrained supply, largely due to the complex containment requirements of high-potency active ingredients. New multi-billion-dollar facilities in Singapore and Shanghai show that firms are internalizing production to safeguard launch timelines. Despite these projects, procurement teams still hedge risk by exploring alternative payload classes that require lower handling stringency. This effort indirectly boosts demand for next-generation linkers capable of accommodating varied chemical moieties, fostering incremental process innovations.
Other drivers and restraints analyzed in the detailed report include:
For complete list of drivers and restraints, kindly check the Table Of Contents.
Enhertu commands 22.80% Antibody Drug Conjugate market share in 2025, and its forecast CAGR of 30.17% indicates continued leadership through 2031. That momentum stems from approvals spanning breast, gastric, and lung cancers, creating a multi-indication revenue stream. Clinical evidence showing superiority over conventional first-line HER2 regimens suggests payers may soon face pressure to broaden front-line coverage.
Adcetris retains relevance in hematology, but an expansion effort into large B-cell lymphoma hints at renewed growth potential. Padcev's combination with pembrolizumab for urothelial cancer has cut mortality risk by nearly half, bolstering uptake in community settings. Emerging assets such as sacituzumab tirumotecan highlight a pipeline tilt toward dual-payload configurations, offering differentiation in refractory disease. Collectively, these products underscore that the Antibody Drug Conjugate market size benefits from both breadth of indications and depth of data in specific cancers.
Cleavable linkers accounted for roughly 69.20% of the Antibody Drug Conjugate market size in 2025, yet site-specific conjugation technologies are set to grow at over 30.08% CAGR through 2031. Exo-cleavable designs offer enhanced systemic stability while ensuring reliable intracellular release, a combination valued by regulators.
Site-specific platforms employing enzymatic or genetic-code expansion methods yield homogeneous drug-antibody ratios that can support lower clinical doses. The trajectory implies manufacturing analytics will shift toward high-throughput DAR confirmation assays, creating new business for specialty contract research organizations. Non-cleavable linkers, while shrinking in share, remain favored for payloads susceptible to premature cleavage, ensuring niche demand persists.
The Antibody Drug Conjugates Market Report Segments the Industry Into by Product Type (Adcetris, Kadcyla, and More), by Application (Blood Cancer, Breast Cancer, and More), by Technology (Clevable Linker, and More), by Target Type (CD30 Antibodies, and More), by End User, and Geography. The Market Sizes and Forecasts are Provided in Terms of Value (USD).
North America accounted for 41.20% of the global Antibody Drug Conjugate market size in 2025, buoyed by early FDA approvals and concentrated research infrastructure. Physician familiarity with biomarker testing ensures rapid patient identification, a factor that compresses adoption lag. The region's reimbursement frameworks now include ADC-specific payment codes, shortening revenue recognition cycles for new launches. As U.S. oncology networks integrate telehealth, follow-up visits for manageable toxicities shift to virtual platforms, freeing clinic capacity.
Asia-Pacific is the fastest-growing territory with a projected CAGR above 31.43% to 2031, driven by rising cancer incidence and supportive national insurance policies. China's inclusion of an ADC in its reimbursement list led to notable upticks in prescription volume, illustrating how policy steers uptake. Indigenous firms are entering global trials, hinting at future export ambitions. Japan's outpatient payment reform underpins hospital economics by incentivizing day-care infusions. A plausible knock-on effect is that regional contract manufacturers specializing in high-potency payloads will attract multinational partnerships, elevating Asia-Pacific's manufacturing clout.
Europe retains meaningful Antibody Drug Conjugate market share, backed by robust health-technology-assessment processes and specialized treatment centers. Germany's outpatient coding adjustments lower hospital overheads, subtly improving jurisdictional competitiveness. The United Kingdom's Cancer Drugs Fund often grants interim access while full evaluation proceeds, shortening patient wait times. Middle Eastern and South American markets, although smaller, exhibit early adoption trends in tertiary centers, signaling future growth pockets. These regions may deploy managed-entry agreements to mitigate budget impact, creating fertile ground for value-based-pricing pilots.