
폴리필 제품 시장은 2025년 334억 6,000만 달러로 평가되었고, 2026년에는 341억 8,000만 달러, 2031년까지 380억 2,000만 달러에 달할 것으로 예측됩니다. 2026년부터 2031년에 걸쳐 CAGR은 2.15%를 나타낼 전망입니다.
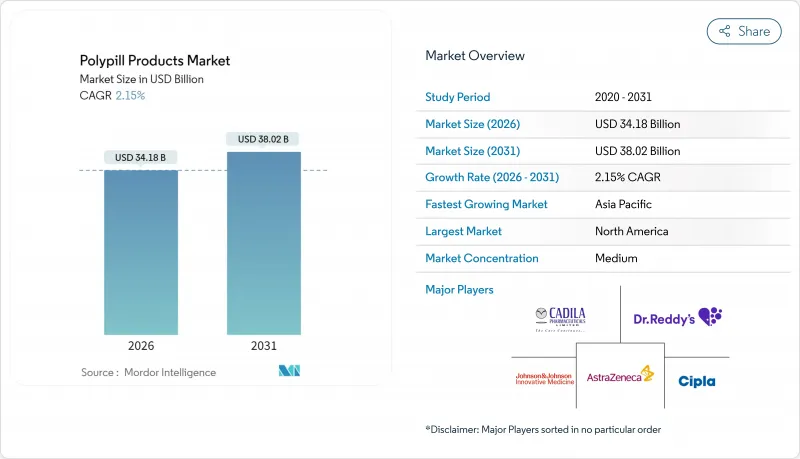
임상적 증거 축적, 세계보건기구(WHO)의 필수 의약품 리스트에 게재, 규제면에서의 지원적 이정표에 의해 고정용량 배합제는 실험적 컨셉에서 주류의 예방 심장병학 툴로 변모를 이루었습니다. 3개 제형 폴리필이 상업적 주도권을 유지하는 반면, 미국에서 처음으로 고혈압 초기 치료용 3제 제제가 승인됨으로써 고정 용량 요법에 대한 의사의 신뢰가 확대되고 있습니다. 지리적 기세는 아시아태평양으로 옮겨가고 있으며 심혈관 질환의 유병률 상승과 인프라 투자가 이 지역에서 가장 강한 성장 전망을 지지하고 있습니다. 경쟁의 심각성은 다국적 혁신 기업과 비용 우위를 지닌 지역 제조업체들이 경쟁하는 동안 여전히 적당합니다. 그러나 최근 승인과 파이프라인에 대한 투자는 특히 초저용량 4개 제제와 디지털 헬스 대응 제품에서 제품 출시 빈도의 가속을 시사하고 있습니다.
미국에서는 약 1억 2,790만 명의 성인(인구의 48.6%)이 적어도 하나의 심혈관 질환을 앓고 있으며, 치료 대상인 환자층은 꾸준히 확대되고 있습니다. 고혈압은 세계에서 12억명 이상에 영향을 미치고 있지만, 주요 경제국의 관리율은 50% 미만으로, 폴리필이 채워지는 지속적인 치료 격차가 존재하는 것을 부각하고 있습니다. 고소득국가의 인구 고령화와 신흥 시장의 도시형 라이프스타일로의 전환이 함께 이 수요 증가세를 지지하고 있습니다. 미국에서는 비히스패닉계 흑인 커뮤니티가 심혈관질환의 부담을 불균형으로 짊어지고 있으며, 간소화된 고정용량요법은 공정성을 중시한 개입책이 됩니다. 의료 시스템이 예방 전략을 강화하는 동안, 단일 정제를 통한 원활한 다기능 제어는 처방 의사의 관심을 끌고 있으며 폴리필 제품 시장의 성장을 뒷받침하고 있습니다.
26건의 무작위 비교 시험의 메타분석은 폴리필 요법이 표준 치료에 비해 사망률을 11% 감소시키고 심혈관 사건을 29% 감소시키는 것으로 나타났습니다. SECURE 시험에서는 2차 예방에 있어서 주요 심혈관 이벤트가 24% 감소, PolyPars 연구에서는 1차 예방 환경에서 리스크가 50% 감소한 것으로 보고되었습니다. 이에 대형제약기업은 파이프라인의 확충으로 대응하고 있습니다. 아스트라제네카는 189개의 심혈관 프로젝트를 보유하고 있으며, 머크는 최근 퍼스트 인 클래스 경구 지단백질(a) 억제제인 HRS-5346의 라이선싱을 받았습니다. 2025년 FDA가 위다프리크를 고혈압 치료의 초기 요법으로 승인함에 따라 폴리필은 최종 수단에서 제1선택약으로 자리를 바꾸고 세계 규제심사의 진행을 가속화했습니다. 이러한 획기적인 진전이 결합되어 과학적·상업적 신뢰성을 높여 폴리필 제품 시장을 전진시키고 있습니다.
구성 약물의 복합 위험 프로파일은 저혈압, 신장 기능에 미치는 영향, 신진 대사 변화에 대한 경계를 높이고 일상적인 약물 모니터링을 복잡하게합니다. 의사는 환자가 부작용을 경험했을 때 개별 복용량 조정에 관심이 있으며, 규제 당국은 집단 규모의 안전 증거를 요구하기 때문에 개발 기간이 장기화되고 있습니다. 시판 후 조사는 어떤 활성 성분이 부작용을 일으켰는지 파악할 필요가 있으며, 이는 복잡한 작업이며 처방 의사를 망설이는 요인이 되어 신중한 시장에서의 단기 보급을 억제할 수 있습니다.
2025년에는 삼제 배합 제제가 매출의 42.70%를 차지했고 종합적인 리스크 인자 커버에 대한 의사의 확고한 신뢰를 나타내, 위다프릭 승인 후의 제일 선택 치료의 기반이 되었습니다. 4제 이상 배합 제제는 4.12%의 연평균 복합 성장률(CAGR)을 나타내며 각 성분의 투여량을 줄임으로써 부작용을 최소화하면서 효과를 유지하는 혁신을 견인하고 있습니다. QUARTET USA 시험에서는 4제 배합 및 1/4 용량 전략이 검증되어 현저한 혈압 저하와 80%의 환자 만족도를 달성했습니다. 이러한 데이터는 점진적 증가에서 즉각적인 다중경로 제어로의 전환을 가속화하고 첨단 의료 모델에서 폴리필 제품 시장 규모를 지원합니다. 듀얼 클래스 및 싱글 클래스 제형은 증량 유연성과 틈새 존재감을 유지하지만, 지침이 다제 배합 정제의 광범위한 채택을 권장하는 동안 점유율은 점차 감소하는 경향이 있습니다.
초저용량 사제 배합정은 내약성의 트레이드오프를 최소화하면서 리스크 인자를 최대한 억제하는 방향으로의 전환을 나타내고 있습니다. 체계적인 검토에서는 목표 혈압 달성률 90%가 확인되고 경미한 유해 사건 프로파일에 의해 치료 중지에 이르는 경우는 드뭅니다. 실제 임상적 인지도가 높아짐에 따라 지불 기관은 입원 회피 효과를 인식하고 4제 배합 폴리필 제품 시장 점유율은 2031년까지 점차 확대될 것으로 전망됩니다.
스타틴+혈압강하제 배합제는 수십년에 걸친 안전성 데이터와 WHO에 의한 아토르바스타틴계 배합제의 권장을 배경으로 2025년에는 32.40%의 점유율을 차지했습니다. 고정 배합제인 아토르바스타틴 + 암로디핀 5/20mg정은 자유 배합제와 비교하여 복합 엔드포인트를 대폭 감소시켜 2차 예방에 있어서의 역할을 확고하게 하고 있습니다. 항혈소판제의 혼입에 의해 리스크 저감 효과가 향상되고, CNIC 폴리필은 2차 예방 용도로 유럽 의약품청(EMA)의 승인을 취득. 삼성분 제제는 현재 3.79%의 연평균 복합 성장률(CAGR)로 확대 중입니다. 특히 저중소득국(LMIC) 입찰의 보급이 진행되고 있는 가운데, 3성분 스타틴 배합 폴리필 제품 시장 규모는 전략적인 확대가 전망됩니다.
새로운 제제로는 스타틴에 PCSK9 억제제와 SGLT2 억제제를 병용하여 잔존하는 지질 대사 위험과 대사 위험에 대처하는 것이 등장하고 있습니다. 한국의 테르미사르탄/로스바스타틴/암로디핀/에제티미브의 4제 배합제 '누보로제트'의 2025년 승인은 지속성 지질이상증이라는 암멧 필요를 대상으로 한 다기서작용형 정제에 대한 규제 당국의 개방성을 나타냅니다. 이러한 혁신은 치료 옵션을 다양화하고 조기 진출기업의 경쟁 우위를 강화합니다.
북미는 2025년 매출의 40.15%를 차지했습니다. 이는 고급 상환제도, 임상시험 인프라 및 제1선택 고혈압 치료에 있어서 Widaplik의 권장에 기인합니다. 미국에는 1억 2,200만 명의 고혈압 성인이 존재하지만, 50% 미만의 관리율은 채택의 큰 여지를 나타냅니다. 캐나다에서는 중앙 집권적인 의약품 심사에 의해 주 수준의 보험 적용이 가속화되고, 멕시코의 세그로 파퓰러 개혁은 고정 용량 조제를 유지하고 있습니다. 지역 연구 개발 거점에서는 QUARTET USA 등의 중요한 데이터 세트가 만들어져 병용 요법의 주류화를 더욱 추진하고 있습니다.
아시아태평양은 확대되는 중산계급 인구, 생활양식의 변화, 1차 케어의 보급 확대로 6.62%라는 가장 빠른 CAGR을 기록하고 있습니다. 인도의 제약기업(심장질환 치료제 포트폴리오가 10% 성장한 Cipla가 대표예)는 국내 시장 및 수출 시장을 위한 가격 경쟁력 있는 공급을 추진하고 있습니다. 중국의 2024년 고혈압 지침은 병용 요법의 유용성을 강조하고 있으며, 한국의 NUVOROZET 승인은 규제 측면에서의 진전을 반영합니다. 일본과 호주는 임상연구 파이프라인과 디지털 헬스 통합을 추진하여 기술 중심 심장병학의 지역적 리더십을 강화하고 있습니다.
유럽, 중동, 아프리카 및 남미는 각각 다른 특성을 가진 기회 환경을 형성합니다. 유럽에서는 유럽 의약품청(EMA)에 의한 CNIC 복합약의 승인이 2차 예방 프로토콜의 기반이 되어 혜택을 받고 있습니다. 나이지리아와 케냐의 조달 파이프라인은 WHO의 필수 의약품 리스트 게재에 의해 추진력을 얻고 있으며, 아르헨티나의 경제적 실현 가능성(월간 치료비가 0.2-2.8일분의 임금에 상당)이 나타나고 있습니다. 시장 진출 전략은 다른 규제, 상환 및 인프라 조건에 대응하는 유연성이 요구되지만, 심혈관 질환 이환율의 상승이 3대륙 전체에서의 지속적인 수요를 지지하고 있습니다.
The Polypill Products Market is expected to grow from USD 33.46 billion in 2025 to USD 34.18 billion in 2026 and is forecast to reach USD 38.02 billion by 2031 at 2.15% CAGR over 2026-2031.
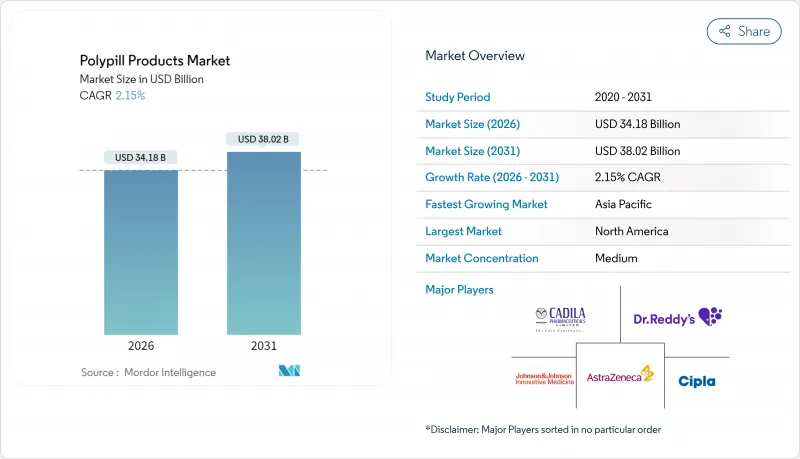
Mounting clinical evidence, the World Health Organization (WHO) essential medicines listing, and supportive regulatory milestones have transformed fixed-dose combinations from experimental concepts into mainstream preventive cardiology tools. Triple-class polypills continue to set the commercial pace, while the first U.S. approval of a triple combination for initial hypertension therapy is widening physician confidence in fixed regimens. Geographic momentum is shifting toward Asia Pacific, where rising cardiovascular prevalence and infrastructure investment underpin the strongest regional growth outlook. Competitive intensity remains moderate as multinational innovators compete with cost-advantaged regional manufacturers. Yet, recent approvals and pipeline investments suggest accelerated product-launch frequency, especially for ultra-low-dose quadruple combinations and digital-health-enabled offerings.
Roughly 127.9 million U.S. adults, 48.6% of the population, now live with at least one cardiovascular condition, creating a steadily enlarging treatment-eligible cohort. Hypertension affects more than 1.2 billion individuals worldwide, yet control rates sit below 50% in significant economies, underscoring a persistent therapeutic gap that polypills can close. Population aging in high-income countries and urban lifestyle shifts in emerging markets together sustain this demand trajectory. Non-Hispanic Black communities in the United States disproportionately carry the cardiovascular burden, making simplified fixed-dose regimens an equity-oriented intervention. As health systems intensify preventive strategies, seamless multi-mechanism control delivered by single tablets is gaining prescriber mindshare, reinforcing growth in the polypill products market.
Meta-analyses of 26 randomized controlled trials now show an 11% mortality reduction and 29% cut in cardiovascular events with polypill therapy versus usual care. The SECURE trial delivered a 24% drop in major adverse cardiovascular events in secondary prevention, while the PolyPars study reported a 50% risk reduction in primary prevention settings. Pharmaceutical majors responded with deeper pipelines; AstraZeneca lists 189 cardiovascular projects and Merck recently licensed HRS-5346, a first-in-class oral lipoprotein(a) inhibitor. The FDA's 2025 clearance of Widaplik as initial hypertension therapy shifted polypills from last-resort status to first-line options, accelerating global regulatory review queues. Collectively, these milestones add scientific and commercial credibility, powering the polypill products market forward.
The combined risk profiles of constituent drugs heighten vigilance over hypotension, renal effects, and metabolic changes, complicating routine pharmacovigilance. Physicians worry about tweaking individual doses once patients encounter side effects, and regulators demand population-wide safety evidence, prolonging development timelines. Post-market surveillance must parse which active agent drives an adverse event complex task that can deter prescribers, dampening near-term uptake in cautious markets.
Other drivers and restraints analyzed in the detailed report include:
For complete list of drivers and restraints, kindly check the Table Of Contents.
Triple-class formulations delivered 42.70% revenue in 2025, illustrating entrenched physician trust in comprehensive risk-factor coverage and serving as anchors for first-line therapy after the Widaplik approval. Quad-or-higher designs post a 4.12% CAGR and spearhead innovation by lowering each component dose to minimize side-effects without efficacy loss. The QUARTET USA trial validated four-drug, quarter-dose strategies, achieving notable blood-pressure reductions and 80% patient satisfaction. These data accelerate clinician migration away from step-wise titration toward immediate multi-pathway control, buttressing the polypill products market size in advanced care models. Dual-class and single-class subsets retain niche relevance for titration flexibility but face gradual share erosion as guidelines endorse broader adoption of multi-class tablets.
Ultra-low-dose quadruple tablets illustrate the shift toward maximized risk-factor suppression with minimized tolerability trade-offs. Systematic reviews show 90% achievement of target blood pressure and mild adverse-event profiles rarely prompting discontinuation. As real-world familiarity grows, payors recognize hospitalization-avoidance benefits, and the polypill products market share of quad-class offerings is set for incremental uptake through 2031.
Statin + antihypertensive formulations held 32.40% share in 2025, underpinned by decades of safety data and WHO endorsement of atorvastatin-based combinations. Fixed atorvastatin + amlodipine 5/20 mg tablets significantly cut composite endpoints versus free combinations, cementing their role in secondary prevention. Incorporating antiplatelets elevates risk-reduction potential; the CNIC polypill secured EMA approval for secondary-prevention use, and triple-component blends now expand at a 3.79% CAGR. As broader access materializes, especially in LMIC tenders, the polypill products market size for triple-class statin combinations is poised for strategic scale.
Emergent formulations include PCSK9 or SGLT2 inhibitors alongside statins, tackling residual lipid and metabolic risk. South Korea's 2025 approval of NUVOROZET, a telmisartan/rosuvastatin/amlodipine/ezetimibe quartet illustrates regulatory openness to multi-mechanism tablets targeting persistent dyslipidemia unmet needs. These innovations diversify therapeutic arsenals and deepen competitive moats for early entrants.
The Polypill Products Market Report is Segmented by Product Type (Single-Class Polypill, Dual-Class Polypill, and More), Composition (Statin + Antihypertensive, and More), Application (Cardiovascular Disease Prevention, and More), Distribution Channel (Hospital Pharmacies, and More), and Geography (North America, Europe, Asia-Pacific, Middle East & Africa, South America). The Market Forecasts are Provided in Terms of Value (USD).
North America supplied 40.15% of 2025 sales, thanks to sophisticated reimbursement, clinical-trial infrastructure, and the Widaplik endorsement for first-line hypertension management. The United States hosts 122 million hypertensive adults, yet under-50% control rates underline substantial headroom for adoption. Canada's centralized drug review accelerates provincial coverage, while Mexico's Seguro Popular reforms sustain fixed-dose procurement. Regional R&D hubs yield pivotal datasets such as QUARTET USA, which further mainstream combination strategies.
Asia Pacific records the fastest 6.62% CAGR on enlarging middle-class demographics, lifestyle shifts, and improving primary-care reach. India's manufacturers, typified by Cipla with 10% cardiac-portfolio growth, drive price-competitive supply for domestic and export markets. China's 2024 hypertension guidelines highlight combination-therapy utility, and South Korea's NUVOROZET approval reflects regulatory momentum. Japan and Australia advance clinical-research pipelines and digital-health integration, reinforcing regional leadership in technology-enabled cardiology.
Europe, the Middle East & Africa, and South America together form a heterogeneous opportunity landscape. Europe benefits from EMA's CNIC-polypill clearance, anchoring secondary-prevention protocols. Procurement pipelines in Nigeria and Kenya gain impetus from WHO's essential medicines listing, while affordability levels in Argentina (0.2-2.8 days' wages for monthly therapy) demonstrate economic feasibility. Market-entry strategies must flex to divergent regulatory, reimbursement, and infrastructure conditions, yet rising cardiovascular morbidity supports sustained demand across all three continents.