
2026년 체외진단약 포장 시장의 규모는 96억 8,000만 달러로 추정되며, 2025년 92억 1,000만 달러에서 성장하여, 2031년에는 123억 8,000만 달러에 이를 것으로 예측됩니다.
2026년부터 2031년까지는 CAGR 5.05%로 성장할 전망입니다.

이 성장세는 자동화 대응 튜브, 사전 검증된 1차 용기, 복잡화하는 분자 검사를 보호하는 콜드체인 수송 용기의 도입 확대를 반영하고 있습니다. 저추출성 폴리머 및 변조 방지 부품에 대한 수요가 공급업체의 제품 포트폴리오를 확대하는 한편, 환경 관리 및 폴리머 조달 가격의 변동이 이익률 관리에 새로운 과제를 가져오고 있습니다. 경쟁은 여전히 중간 정도로 상승세에 있으며, 수직 통합 기업이 독자적인 항응고제, 사전 바코드 라벨, 저스트 인 타임 서비스를 결합하여 실험실 계약을 확보하고 있습니다. 한편, 유리 고분자 하이브리드와 초저추출 공중합체는 고처리량 분자 워크플로에서 고부가가치 틈새 시장을 개척하고 있습니다. 게다가, 가정용 검사나 분산형 검체 채취를 촉진하는 지역적인 환급제도 개혁에 의해 최종 사용자의 다양화가 진행되어, 사용 용이성과 상온 안정성에 최적화된 포장 형태의 개발이 추진되고 있습니다.
2024년 미국 의료보험서비스센터(CMS)가 발행한 확대 환급코드는 지속혈당 모니터와 응고검사 스트립을 새롭게 환급 대상으로 지정하였고, 이는 콜드체인 제약을 방지하는 샘플 안정화제를 내장한 일회용 디바이스에 대한 수요를 환기하고 있습니다. 식품의약국(FDA)이 최종화한 가정용 표시에 관한 지침에서는 픽토그램에 의한 설명과 어린이 보호 캡이 의무화되어, 용기의 재설계나 다언어 디지털 인쇄기에 대한 투자가 촉구되고 있습니다.
미국 및 유럽의 약국 체인은 자동 판매기에서 신속 검사 키트를 판매하기 시작했으며, 따라서 습도 변화와 반복적인 취급에 대한 내성을 갖춘 포장에 대한 요구가 더욱 커지고 있습니다. 지불자 지원, 규제의 명확화, 소매 유통의 확대가 더해, 가정용 검사 포장의 2자리수 성장이 지속되고 있습니다.
지멘스 헬시니어스의 Atellica 자동화 플랫폼을 도입한 연구소에서는 처리 시간을 약 30% 단축하고 있으나, 로봇에 의한 취급에도 견딜 수 있는 엄격한 치수 공차와 기계 판독 가능한 라벨을 갖춘 시험관의 조달이 필요합니다. 차세대 시퀀싱 워크플로는 DNA 손실을 최소화하는 저흡착성 폴리프로필렌 플레이트를 선호하며, 공급업체는 표면 개질 폴리머의 개발을 추진하고 있습니다. ISO 15189 인증 획득은 추적성 요건을 강화하고, 실험실은 저사양 범용품을 제외한 사전 검증된 소모품에 대한 투자를 추진하고 있습니다. 그 결과, 자동화 대응 형식은 기존 벤더에 대한 지출 집중을 촉진하고 있습니다.
EU의 일회용 플라스틱 지침에서는 의료기기가 제외되고 있지만, 의료 시스템에서는 자발적으로 폐기물 저감에 임하고 있으며, 영국 국민 보건 서비스(NHS)는 2028년까지 25% 저감을 내세우고 있습니다. 2024년에 발행된 ISO 18604는 제조업자에게 재생재료 함량 공개와 재활용성을 고려한 설계를 의무화하고 있으며, 이는 개발 사이클의 연장과 컴플라이언스 비용 증가를 가져오고 있습니다. 독일 벡톤디킨슨의 재활용 프로그램과 같은 시험적 회수 계획은 관심의 높이를 보여주지만, 생물학적 위험물의 오염 제거 및 비용면에서 장벽이 존재합니다. 재생 등급 폴리프로필렌의 프리미엄 가격과 재검증 요구도 도입을 더욱 억제하는 요인이 되고 있습니다.
폴리프로필렌은 2025년 매출액의 40.84%를 차지하였고 혈청 분리 튜브, 소변 용기, 범용 시약 용기에서 주력 소재로서의 지위를 강화했습니다. 환상 올레핀계 공중합체(COC)는 마이크로플루이딕스 카트리지 및 단일 사용 바이오리액터에 적합한 초저추출 특성과 광학 투명성을 바탕으로 2031년까지 연률 6.12%의 성장이 예상됩니다. Topas Advanced Polymers는 자동 처리 시 파손을 최소화하는 프리필드 시약 카세트에 대한 수요로 인해 IVD 기업용 COC 출하량이 40% 급증했다고 보고했습니다. 폴리에틸렌 테레프탈레이트는 뛰어난 방습성으로 시약 완충액 병의 주력 소재로 유지되고 있습니다. 한편, 붕규산 유리는 매우 높은 화학적 불활성 특성이 요구되는 틈새 용도로 도입되고 있습니다.
분자진단 플랫폼이 시료 준비, 증폭, 검출을 컴팩트한 일회용 카트리지와 통합함에 따라 COC의 기세는 더욱 가속될 전망입니다. 스테바나토 그룹의 EZ-Fill 포맷은 이러한 동향을 구현하고 있으며, COC 본체에 바늘과 바코드를 일체화하여 분속 300유닛을 넘는 라인 속도를 실현하고 있습니다. 폴리프로필렌 공급업체는 투명성을 높인 공중합체로 대응하고 있지만, 재인증 비용과 수지 가격 상승이 보급을 늦추고 있습니다. 예측 기간에는 성능 요구사항, 규제 준수 및 총 소유 비용이 체외진단약 포장 시장에서 COC가 기존 재료를 대체하는 속도를 결정할 것입니다.
튜브는 2025년에 제품 유형별 매출의 38.25%를 차지했고, 진공 채혈의 보급과 마이크로 채혈 디바이스에 의존하는 포인트 오브 케어 검사의 확대가 이를 견인했습니다. 캡류는 6.49%의 연평균 복합 성장률(CAGR)로 가장 빠른 성장이 예상되며 변조 방지 기능과 어린이 보호 기능을 요구하는 FDA 및 EU의 신규 안전 기준이 촉진요인이 됩니다. 벡톤디킨슨의 헤모가드 밀봉 장치는 2024년에 회사 채혈 수익의 60% 이상을 차지했으며, 안전성 향상으로 인한 프리미엄 가격화를 돋보이게 했습니다. 바이알과 병은 동결건조 시약의 보존과 벌크 시약 공급에 중요한 역할을 하는 반면, 통합형 샘플링 장치는 환자의 편의성과 검사실의 자동화를 모두 실현합니다.
개정된 ISO 8317 토크 및 어린이 보호 프로토콜을 통해 공급업체는 푸시 앤 턴 또는 스퀴즈 앤 턴 캡을 설계해야 하므로 성형의 복잡성과 단가가 증가합니다. 웨스트 파머슈티컬 서비스의 컬러 체인지 플립오프 씰은 보관 연속성이 중요한 법의학 및 도핑 검사에서의 이용 사례를 목적으로 하고 있습니다. 분자 워크플로용으로 설계된 튜브는 증발 방지를 위해 더 높은 밀봉 무결성을 필요로 하는 안정화 시약이 포함되는 경우가 증가하고 있습니다. 안전성, 규제, 기능성의 요구가 융합됨에 따라 체외진단약 포장 시장 전체에서 마개는 범용품에서 부가가치 부품으로 격상되고 있습니다.
북미는 2025년에도 39.50%의 수익 점유율을 유지했습니다. 이는 높은 검사 실행률, 정착된 자동화 프로세스, 엄격한 규제 프레임워크가 기존 공급업체의 지위를 확고하게 했기 때문입니다. 시장 기업은 지정학적 위험에 대한 헤지와 지역 조달을 권장하는 주 수준의 법규에 대응하기 위해 국내 튜브 생산 능력을 확충하고 있습니다. 캐나다의 공공 조달에서는 IVD 소모품에 대한 UDI 추적성이 의무화되어 미국 FDA의 기준을 준수함과 동시에 직렬화된 용기에 대한 수요를 강화하고 있습니다. 이 지역의 가정용 진단과 만성 질환 모니터링에 대한 주력은 변조 방지 기능이 있는 마개와 상온 안정성을 겸비한 일회용 키트의 수주를 가속시키고 있습니다.
아시아태평양은 가장 빠른 성장 궤도를 보이며 2031년까지 7.68%의 성장이 예상됩니다. 중국은 2027년까지 공공병원에 분자진단 능력을 도입하는 정책을 통해 시험관, 시약 카트리지, 콜드체인 수송 용기의 대량 수요를 창출할 전망입니다. 벡톤디킨슨의 1억 5,000만 달러 규모의 소주 공장 확장은 이러한 수요 획득을 위한 공급업체의 움직임을 상징합니다. 인도의 국가 보건 미션이 검사실 설비 업그레이드에 500억 루피(6억 달러)를 할당한 사례도 자동화 대응 용기의 도입을 촉진하고 있습니다. 지역 성장은 NMPA 승인을 취득한 현지 제조업체의 대두에 의해 가속화되고 있습니다. 경쟁이 심화되는 반면 대량 생산 플라스틱 제품 공급망은 축소되었습니다.
유럽에서는 2024년에 완전 시행된 의료기기 규칙(MDD)과 체외진단용 의료기기 규칙(IVDR) 하에서 안정적인 성장을 보여주고 있습니다. 이들은 UDI 인코딩 바코드와 시판 후 조사를 의무화하면서 컴플라이언스 비용을 밀어 올리고 있습니다. Shot AG가 중국에 1억 유로(1억 900만 달러)를 투입한 유리관 공장은 유럽 기지의 검사 키트 공급업체가 아시아 충전 현장에 가까운 곳에서 적합한 바이알을 조달할 수 있게 합니다. 영국은 브렉시트 후 규제 분기로 이중 적합성 평가가 추가되어 공급업체 시장 투입 기간이 연장되는 한편 국내 혁신이 촉진되고 있습니다. 남미의 근대화 프로그램과 아프리카 연합의 공동 조달 플랫폼은 점진적인 성장을 보장하지만 통화 변동과 단편화된 콜드체인 인프라에 직면하고 있습니다. 세계 전개를 계획하는 공급업체는 체외진단약 포장 시장 전체에서 획일적인 전략을 채택하는 것이 아니라, 현지의 규제 및 물류 성숙도에 따라 시장 진출 전략을 조정하고 있습니다.
The in-vitro diagnostics packaging market size in 2026 is estimated at USD 9.68 billion, growing from 2025 value of USD 9.21 billion with 2031 projections showing USD 12.38 billion, growing at 5.05% CAGR over 2026-2031.
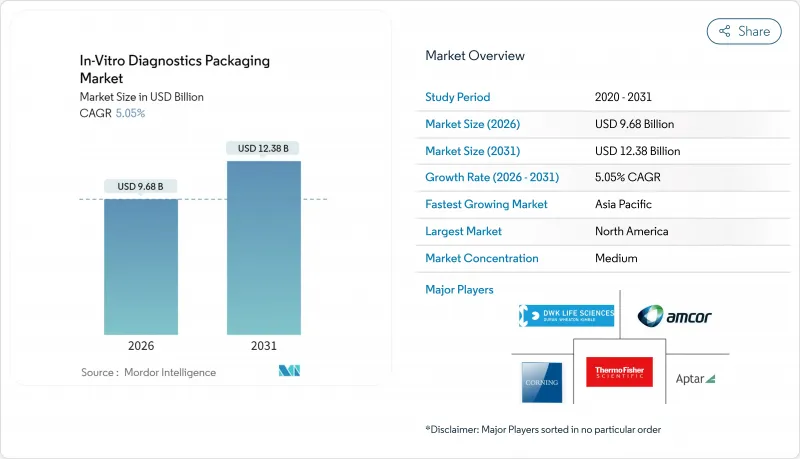
This momentum reflects growing adoption of automation-ready tubes, pre-validated primary containers, and cold-chain shippers that safeguard increasingly complex molecular assays. Demand for low-extractable polymers and tamper-evident components is broadening supplier portfolios, while environmental stewardship and polymer-sourcing volatility inject fresh challenges into margin management. Competitive intensity remains moderate yet is rising, as vertically integrated players combine proprietary anticoagulants, pre-bar-coded labeling, and just-in-time services to secure laboratory contracts. Meanwhile, glass-polymer hybrids and ultra-low extraction copolymers are carving high-value niches within high-throughput molecular workflows. In parallel, regional reimbursement reforms that favor at-home testing and decentralized sample collection are expanding end-user diversity, driving the development of packaging formats optimized for user friendliness and ambient stability.
Expanded reimbursement codes issued by the Centers for Medicare and Medicaid Services in 2024 now cover continuous glucose monitors and coagulation strips, spurring demand for single-use devices with integrated sample stabilizers that sidestep cold-chain constraints. The Food and Drug Administration's finalized guidance on home-use labeling requires pictogram instructions and child-resistant closures, prompting redesign of containers and investment in multilingual digital presses.
Pharmacy chains across the United States and Europe have begun stocking rapid tests in vending kiosks, further taxing packaging to withstand the effects of humidity shifts and repeated handling. Together, payer support, regulatory clarity, and retail distribution are sustaining double-digit growth in at-home test packaging.
Laboratories adopting Siemens Healthineers' Atellica automation platform reduce turnaround times by approximately 30%, yet must source tubes with strict dimensional tolerances and machine-readable labels that withstand robotic handling. Next-generation sequencing workflows favor low-bind polypropylene plates that minimize DNA loss, steering suppliers toward surface-modified polymers. ISO 15189 accreditation enhances traceability requirements, prompting labs to invest in pre-validated consumables that exclude lower-specification generics. As a result, automation-ready formats are consolidating spend with established vendors.
Although the EU Single-Use Plastics Directive exempts medical devices, health systems voluntarily target waste reduction, with the UK National Health Service pledging a 25% cut by 2028. ISO 18604 issued in 2024 obliges manufacturers to disclose recycled content and design for recyclability, extending development cycles and compliance costs. Pilot take-back schemes, such as Becton Dickinson's German recycling program, illustrate interest yet highlight biohazard decontamination and cost hurdles. Recycled-grade polypropylene premiums and revalidation demands further temper adoption.
Other drivers and restraints analyzed in the detailed report include:
For complete list of drivers and restraints, kindly check the Table Of Contents.
Polypropylene captured 40.84% of 2025 revenue, reinforcing its status as the workhorse substrate for serum-separator tubes, urine containers, and general reagent vessels. Cyclic olefin copolymer is forecast to grow 6.12% annually through 2031, underpinned by its ultra-low extractables profile and optical clarity that favor microfluidic cartridges and single-use bioreactors. Topas Advanced Polymers registered a 40% surge in COC shipments to IVD firms, citing demand for pre-filled reagent cassettes that minimize breakage during automated handling. Polyethylene terephthalate remains the go-to material for reagent and buffer bottles, thanks to its superior moisture-barrier properties, while borosilicate glass holds niche applications requiring extreme chemical inertness.
COC momentum will likely accelerate as molecular diagnostics platforms integrate sample preparation, amplification, and detection into compact, disposable cartridges. Stevanato Group's EZ-Fill format exemplifies this trend, pairing COC bodies with integrated needles and barcodes at line speeds exceeding 300 units per minute. Polypropylene suppliers are countering with clarity-enhanced copolymers; however, requalification costs and higher resin prices slow uptake. Over the forecast horizon, performance needs, regulatory compliance, and total cost of ownership will determine the pace at which COC displaces incumbent materials in the in-vitro diagnostics packaging market.
Tubes commanded 38.25% of product-type revenue in 2025, driven by the adoption of vacuum blood collection and the expansion of point-of-care testing that relies on micro-collection devices. Closures are expected to register the fastest advance at a 6.49% CAGR, driven by new FDA and EU safety mandates that require tamper-evident and child-resistant features. Becton Dickinson's Hemogard closure claimed more than 60% of the company's blood-collection revenue in 2024, underscoring how incremental safety can capture premium pricing. Vials and bottles supply critical roles in lyophilized reagent storage and bulk-reagent delivery, while integrated sampling devices bridge patient convenience and lab automation.
Revised ISO 8317 torque and child-resistance protocols require suppliers to engineer push-and-turn or squeeze-and-turn caps, which increase molding complexity and unit cost. West Pharmaceutical Services' color-change flip-off seal targets forensic and doping control use cases where the chain of custody matters. Tubes designed for molecular workflows are increasingly incorporating stabilizer reagents that require higher seal integrity to prevent evaporation. The convergence of safety, regulatory, and functional needs is elevating closures from commodity to value-added components across the in vitro diagnostics packaging market.
The In-Vitro Diagnostics Packaging Market Report is Segmented by Material Type (Polypropylene, Polyethylene Terephthalate, Borosilicate Glass, and More), Product Type (Bottles, Vials, Tubes, and More), Packaging Format (Primary Packaging, Secondary Packaging, and Tertiary Packaging), End User (Hospitals, Diagnostic Laboratories, and More), and Geography. The Market Forecasts are Provided in Terms of Value (USD).
North America maintained a 39.50% revenue share in 2025 as high testing rates, entrenched automation, and stringent regulatory frameworks entrenched incumbent suppliers. Market players continue to expand domestic tube capacity to hedge against geopolitical risk and meet state-level legislation that favors local sourcing. Canada's public procurement now stipulates UDI traceability for IVD consumables, mirroring U.S. FDA alignment and reinforcing demand for serialized containers. The region's emphasis on at-home diagnostics and chronic disease monitoring accelerates orders for single-use kits that combine tamper-evident closures with ambient stability.
The Asia-Pacific region shows the fastest trajectory, projected to grow at 7.68% through 2031. China's policy requiring county hospitals to deploy molecular capabilities by 2027 will generate a high volume of tubes, reagent cartridges, and cold-chain shippers. Becton Dickinson's USD 150 million Suzhou expansion exemplifies supplier moves to capture this demand. India's National Health Mission allocation of INR 50 billion (USD 600 million) for lab upgrades likewise stimulates the adoption of automation-ready containers. Regional growth is amplified by local manufacturers receiving NMPA approvals, which intensifies competition while shortening supply chains for high-volume plastics.
Europe demonstrates stable growth under the Medical Device and In Vitro Diagnostic Regulations that took full force in 2024, demanding UDI-encoded bar codes and post-market surveillance that elevate compliance cost. Schott AG's EUR 100 million (USD 109 million) glass tubing plant in China enables European-based assay vendors to source compliant vials closer to Asian filling sites. The United Kingdom's post-Brexit divergence adds dual conformity assessments, extending time-to-market for suppliers but also fostering domestic innovation. South America's modernization programs and the African Union's pooled procurement platform promise incremental growth but face currency volatility and fragmented cold-chain infrastructure. Suppliers planning global expansion now calibrate go-to-market tactics to local regulatory and logistics maturity rather than adopting uniform strategies across the in-vitro diagnostics packaging market.