
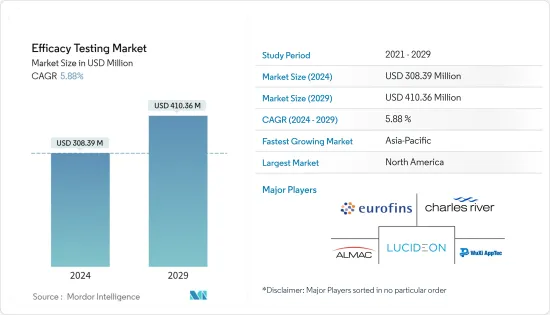
유효성 시험 시장 규모는 2024년 3억 839만 달러로 추정되고 2029년까지 4억 1,036만 달러에 이를 것으로 예측되며 복합 연간 성장률(CAGR) 5.88%로 성장할 전망입니다.
신형 코로나바이러스 감염(COVID-19)의 유행성 발병으로 백신, 의약품 및 기타 의약품과 같은 의약품에 대한 효능 시험이 실시되었습니다. 대규모 고객 기반으로 가정 내 COVID-19의 확산을 방지하기 위해 소독 제품의 판매가 가속화되고 있습니다. 그래서 여러 연구소와 기업들이 제품의 유효성 시험을 실시했습니다. 2022년 10월의 ARIC 기사에 따르면, 알코올 기반의 손가락 소독제(ABHS)가 손가락 소독의 골드 표준으로 간주되고 있지만, ABHS에 필요한 pH, 점도, 과산화수소 함량은 제품의 기능과 관련된 몇 가지 매개 변수입니다. 그리고 사용자로부터의 용이성. 따라서 제품의 유효성과 안전성에 주의를 기울여 관리해야 합니다. 이로 인해 유행 중 검사의 효과가 높아졌습니다. 게다가, 현재는 COVID-19 감염의 백신 연구 개발(R&D) 증가에 따라 의약품의 생산도 증가하고 있습니다. 이로 인해 의약품의 유효성 시험에 대한 수요가 생겨 궁극적으로 시장 성장을 가속합니다.
조사된 시장의 성장은 제약 부문에 의한 R&D 아웃소싱 증가와 품질에 따른 설계(QbD) 접근법의 채용 증가와 같은 요인에 의해 주로 야기될 수 있습니다.
아웃소싱은 제약 부서의 조직이 운영 비용과 제조 비용을 모두 줄여 재무 위험을 최소화하는 데 도움이 됩니다. 이 때문에 제약기업은 R&D 활동을 실시하는 전략으로 R&D 활동을 민간 수탁조사기관(CRO)에 위탁하는 경우가 늘고 있습니다. 예를 들어, 2022년 9월 임상 단계의 생명공학 기업인 Emyria Limited는 신경과학의 전임상 창약 및 수탁조사 조직(CRO)인 PsychoGenics와 제휴했습니다. 이 제휴하에 Emyria는 PsychoGenic의 창약 플랫폼인 차세대 자동 검사 플랫폼인 SmartCube를 사용합니다. 이러한 사례는 유효성 테스트 제품 수요가 증가할 것으로 예상되며, 따라서 예측 기간 동안 시장 성장에 기여할 것으로 예상됩니다.
또한 QbD 접근법을 채택하는 것은 분석 및 위험 관리를 사용하여 품질을 향상시키는 것을 목표로 한 의약품 개발에 대한 체계적인 접근이 가능해지고 효능 시험 기능이 향상되기 때문입니다. 입니다. 따라서 효능 시험 중에 QbD 접근법을 도입하면 개발 능력, 속도 및 배합 설계가 강화됩니다. 게다가 2021년 12월에 AAPS 오픈 액세스 저널에 게재된 기사에 따르면 QbD 전략은 제품과 프로세스의 전문지식 향상, 신뢰성 높은 제조 공정, 의약품에 관한 규제의 유연성 등 의약품 개발에 다양한 이점이 있는 것으로 알려져 있습니다. 안전성과 유효성 테스트에 중점을 두고 상업 단계 전반에 걸쳐 조정합니다. 따라서 유효성 시험 수요가 증가하고 있습니다.
게다가 IFPMA의 2021년 보고서에 따르면 바이오의약품산업의 연간 연구개발 지출은 항공우주산업과 방위산업의 7.3배, 화학산업의 6.5배, 소프트웨어와 컴퓨터서비스산업의 1.5배가 되고 있습니다. 위의 동일한 출처는 바이오 의약품 산업이 2021년에 1,960억 달러를 소비했으며, R&D 활동으로 인해 2024년까지 2,130억 달러로 증가할 것으로 예상된다고 밝혔습니다. 바이오 의약품 업계에서 의약품 개발의 연구 개발이 증가함에 따라 시장 관계자들 사이에서 QbD 접근법의 채택이 증가하고 있습니다. 이로 인해 시장 성장이 기대됩니다. 그러나 테스트 절차에 많은 시간을 소비하는 것이 성장 장애가 될 수 있습니다.
응용 분야별 화장품 및 개인 관리 제품은 예측 기간 동안 상당한 성장을 이룰 것으로 예상됩니다. 화장품의 임상시험은 화장품의 성능과 안전성을 검증할 뿐만 아니라 패키징과 마케팅에 큰 권위와 신뢰성을 부여합니다. 또한 화장품 및 퍼스널케어 제품의 사용량이 증가함에 따라 이러한 제품의 유효성 테스트에 대한 수요가 증가하고 있으며,이 부문의 성장을 추진하고 있습니다.
화장품 및 퍼스널케어 제품에 대한 소비자의 구매 행동은 유행 기간 동안 크게 증가하고 예측 기간 동안 지속될 것으로 예상됩니다. 따라서 일부 기업은 화장품의 유효성 시험에 주력하고 있습니다. 예를 들어 Codex Beauty는 2021년 2월에 소비자가 테스트 프로세스와 제품 주장을 이해할 수 있도록 소비자를 위한 유효성 테스트 라벨을 출시했습니다. Codex Beauty Labs는 향후 제품 라벨에 읽기 쉬운 유효성 테스트 패널을 표시하여 제품 테스트 뒤에 있는 정량적 데이터를 설명할 예정입니다.
또한, 효능 시험은 화장품 제품의 연구 개발에 사용되는 일련의 방법으로, 패키지 또는 마케팅에서의 주장을 검증하고 제품의 사용 목적을 테스트하기 위해 수행됩니다. 또한 소비자의 피부에 직접 사용해도 안전한 화장품임을 확인하기 위해 화장품의 방부제 효력 시험도 실시했습니다. 그러므로 시험 규정은 필수적이며, 이로 인해 화장품 제품의 유효성 시험의 많은 기회가 탄생했습니다. 예를 들어(2021년) 5월에 중국의 화장품 효능 주장 평가 기준이 발효되었습니다. 이에 따르면, 효능 효과를 구하는 화장품은 효능 평가에 의해 뒷받침되는 것으로 되어 있습니다. 기준에 따라 유효성 평가 결과의 개요는 미국 의약품 협회(NMPA)가 지정한 온라인 플랫폼을 통해 공개됩니다. 제품의 유효성은 화장품의 안전성 및 기술 기준에서 필수 시험 기준의 대상이 됩니다.
북미는 예측 기간 동안 전체 유효성 시험 시장을 지배할 것으로 예상됩니다. 연구개발 증가와 이 지역 시장 선수들 사이의 QbD 접근법의 채택과 같은 요인들이 시장 성장을 가속할 것으로 예상됩니다.
북미 제약 산업은 의약품 개발을 위해 CRO로 아웃소싱 활동에 더 중점을 둡니다. 게다가 이 지역 정부는 개발,제조 수탁 조직(CDMO), 원약 및 의약품의 제조 능력에도 많은 투자를 하고 있습니다. 최근 HHS는 잠재적인 COVID-19 바이러스 감염 백신과 치료제의 생산 능력과 생산 능력을 향상시키기 위해 에머전트 바이오 솔루션에 많은 투자를했습니다. 또한, Emergent Bio Solutions는 AstraZeneca의 COVID-19 감염 백신 후보의 제조 파트너가 되는 계약을 AstraZeneca와 체결했습니다. 이러한 CRO 활동은 예측 기간 동안 시장 성장을 가속할 것으로 예상됩니다.
게다가 이 지역에서 확립된 제약산업의 존재, 고액의 연구개발비, 대기업 서비스 제공업체의 강력한 존재감, 그리고 이 지역에서의 제약회사나 화장품회사에 의한 분석시험의 아웃소싱 경향 증가가 이에 기여하는 몇 가지 주요 요인입니다. 시장 전체의 성장으로 이어집니다. 예를 들어 OECD의 2022년 10월 최신 정보에 따르면 미국, 캐나다, 멕시코의 의약품 지출은 각각 2.08, 1.72, 1.34(GDP) 비율입니다. 이는 대기업, 제조업체, 정부기관이 제품 개발에 깊이 관여하고 있음을 보여줍니다. 이에 따라 지역 각국에서 유효성 시험 서비스에 대한 수요가 높아져 조사 대상 시장 전체의 성장이 촉진됩니다.
게다가 FDA에 의한 2021년 8월 최신 정보에 따르면, 가장 안전하고 최첨단 의약품 시스템에 대한 접근은 미국 소비자에게 이익을 가져오기 때문에 이 지역에서의 의약품 개발이 증가하고 있습니다. 게다가, 위의 정보 근거에 따르면, 제약 회사가 미국에서 약을 판매하기 전에, 그 약은 시험을 받아야 합니다. 의약품이 안전하고 의도된 목적에 효과적임을 입증하기 위해, 제조자는 이 시험의 결과를 CDER에 제공합니다. CDER는 의약품을 직접 시험하지는 않지만 의약품의 품질, 안전성 및 효능 기준에 대한 조사를 실시했습니다. 의약품을 검사하는 이러한 규제기관의 존재는 국내에서 조사되는 시장의 성장을 가속할 것으로 예상됩니다.
효능 시험 시장의 경쟁은 적당합니다. 주요 시장 기업은 자체 개발과 기술 인수를 통해 제품 포트폴리오를 확대함으로써 서로 경쟁하고 있습니다. 현재 여러 회사가 시장을 독점하고 있습니다. 이들 기업에는 Eurofins Scientific, Charles River Laboratories, Lucideon Limited, WuXi Apptec 및 Almac Group이 포함됩니다. 주요 기업은 세계 시장에서의 지위를 확보하기 위해 인수, 제휴, 고급 서비스 출시 등 다양한 전략적 제휴에 관여해 왔습니다.
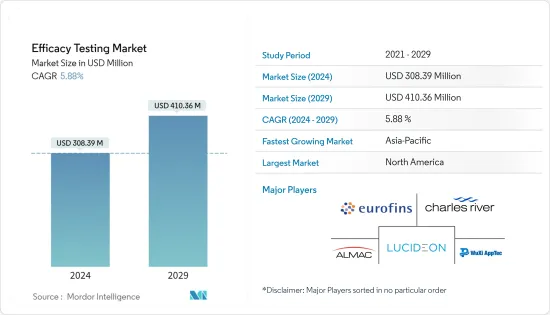
The Efficacy Testing Market size is estimated at USD 308.39 million in 2024, and is expected to reach USD 410.36 million by 2029, growing at a CAGR of 5.88% during the forecast period (2024-2029).
The onset of the COVID-19 pandemic garnered efficacy testing for pharmaceutical products such as vaccines, drugs, and other medical products. A large customer base has fueled the sales of disinfecting products to prevent the spread of COVID-19 in their households. Thus, several laboratories and companies conducted efficacy testing of products. According to an October 2022 ARIC article, alcohol-based hand sanitizers (ABHS) were considered the gold standard for hand disinfection, but the required pH, viscosity, and hydrogen peroxide content of ABHS are a few parameters that are related to the products' functionality and acceptability by the users. Therefore, paying attention to and exercising control over the product's efficacy and safety is necessary. This increased the efficacy of testing during the pandemic. Additionally, in current times, the production of pharmaceutical products has increased, with an increase in research and development (R&D) of COVID-19 vaccines and drugs. This creates demand for efficacy testing of pharmaceutical products, ultimately fueling the market growth.
The studied market growth can largely be attributed to the factors such as an increase in outsourcing of research and development by the pharmaceutical sector and increasing adoption of the quality by design (QbD) approach.
Outsourcing assists organizations in the pharmaceutical sector to reduce both their operational and manufacturing costs and thereby minimize financial risk. Thus, pharmaceutical companies are increasingly outsourcing R&D activities to private contract research organizations (CROs) as a strategy for conducting research and development activities. For instance, in September 2022, Emyria Limited, a clinical-stage biotechnology company collaborated with PsychoGenics, a neuroscience preclinical drug discovery and contract research organization (CRO). Under this collaboration, Emyria uses PsychoGenic's drug discovery platform, SmartCube, which is a next-generation automated testing platform. Such instances are expected to increase the demand for efficacy testing products, and hence, it is anticipated to contribute to market growth over the forecast period.
Additionally, the QbD approach is adopted because it improves the functionality of efficacy testing by allowing for a systematic approach to drug development intended to enhance the quality by using analytical and risk management. Thus, the implementation of the QbD approach during efficacy testing enhances the development capability, speed, and formulation design. In addition, according to an article published in December 2021 in the AAPS open-access journal, the QbD strategy is known to have various benefits for the development of pharmaceutical products, including improved product and process expertise, reliable manufacturing processes, and regulatory flexibility regarding adjustments throughout the commercial phase with a significant focus on safety and efficacy testing. Thus, the demand for efficacy testing is increasing.
Moreover, according to the IFPMA's 2021 report, the annual R&D spending by the biopharmaceutical industry is 7.3 times higher than that of the aerospace and defense industries, 6.5 times more than the chemicals industry, and 1.5 times more than the software and computer services industry. The same source above also mentioned that the biopharmaceutical industry spent USD 196,000 million in 2021 and it is expected to increase to USD 213,000 million by 2024 over research and development activities. With increasing R&D in the biopharmaceutical industry for pharmaceutical product development, the adoption of the QbD approach is increasing among market players. This is expected to garner market growth. However, the high investment of time in testing procedures is likely to be an obstacle to growth.
The cosmetics and personal care products by application segment is anticipated to witness significant growth over the forecast period. The clinical testing of cosmetic products not only verifies the performance and safety of the cosmetic items but also gives its packaging and marketing greater authority and credibility. Moreover, with the increasing usage of cosmetics and personal care products, the demand for the efficacy testing of these products is increasing and further driving the segment growth.
Consumers' buying behavior for cosmetics and personal care products increased significantly during the pandemic and is anticipated to persist over the forecast period. Therefore, several companies are focusing on the efficacy testing of cosmetic products. For instance, in February 2021, Codex Beauty launched a consumer-facing efficacy testing label to help consumers understand its testing process and product claims. Codex Beauty Labs will display an easy-to-read efficacy testing panel on the labels of future products to explain the quantitative data behind product testing.
Moreover, efficacy testing is a series of methods used in cosmetics product research and development and is carried out to verify the claims made on packaging or in marketing and to test the product's intended use. Additionally, to make sure that the cosmetic items are safe for consumers to use directly on their skin, preservative efficacy tests are also carried out on cosmetic products. Thus, the regulation of the tests is mandatory, and this is creating numerous opportunities for cosmetics product efficacy testing. For instance, in May 2021, China's Standards for Cosmetic Efficacy Claim Evaluation came into effect. According to it, cosmetic products with efficacy claims shall be supported by an efficacy evaluation. As per the standards, a summary of efficacy evaluation results will be made available to the public through an online platform specified by the National Medical Products Association (NMPA). The efficacy of products will be subject to the mandatory test standard in the safety and technical standards for cosmetics.
North America is expected to dominate the overall efficacy testing market throughout the forecast period. Factors such as increasing R&D and adoption of the QbD approach among the market players in the region are predicted to drive market growth.
The pharmaceutical industry in North America is focusing more on outsourcing activities to CROs for drug development. In addition, governments across the region are also investing heavily in contract development and manufacturing organizations (CDMO), drug substance, and drug product manufacturing capacities. Recently HHS invested a hefty sum in Emergent BioSolutions to advance manufacturing capabilities and manufacturing capacity for a potential COVID-19 vaccine as well as therapeutics. In addition, Emergent BioSolutions signed an agreement with AstraZeneca to become the manufacturing partner for AstraZeneca's COVID-19 vaccine candidate. These CRO activities are anticipated to fuel market growth over the forecast period.
Furthermore, the presence of a well-established pharmaceutical industry in the region, the high R&D expenditure, the strong presence of major service providers, and the growing trend of outsourcing analytical testing by pharmaceutical and cosmetic companies in the region are several major factors that contribute to the overall market growth. For instance, according to the October 2022 update by OECD, pharmaceutical spending in the United States, Canada, and Mexico is 2.08, 1.72, and 1.34 (% of gross domestic product (GDP)), respectively. This shows the high involvement of major players, manufacturers, and government organizations in product development. This drives demand for efficacy testing services in countries across the region thereby driving the overall growth of the studied market.
Furthermore, according to the August 2021 update by FDA, access to the safest and cutting-edge pharmaceutical system benefits American consumers, thus pharmaceutical product development is increasing in the region. In addition, according to the source mentioned above, a drug must undergo testing before a pharmaceutical company may sell it in the United States. To demonstrate that the drug is safe and effective for its intended purpose, the manufacturer subsequently provides CDER with the results of these testing. Although CDER doesn't directly test pharmaceuticals, it undertakes some research on criteria for drug quality, safety, and effectiveness. The presence of such regulatory bodies to inspect pharmaceutical products is anticipated to fuel the studied market growth in the country.
The efficacy testing market is moderately competitive. Major market players are competing against each other by expanding their product portfolios through in-house development or technological acquisitions. A few companies currently dominate the market. These companies include Eurofins Scientific, Charles River Laboratories, Lucideon Limited, WuXi Apptec, and Almac Group. The key players have been involved in various strategic alliances such as acquisitions, collaborations, and the launch of advanced services to secure their position in the global market.