
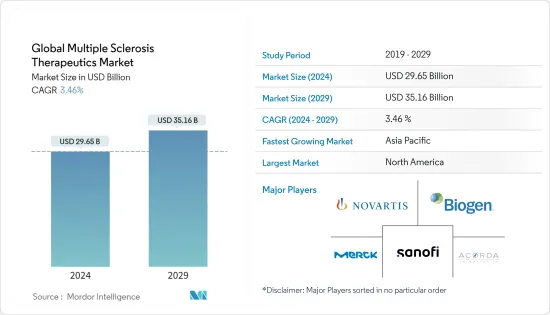
다발성 경화증 치료제 세계 시장 규모는 2024년에 296억 5,000만 달러로 추정되고, 2029년에는 351억 6,000만 달러에 이를 것으로 예측되며, 예측 기간(2024-2029년)의 CAGR은 3.46%로 성장할 전망입니다.
COVID-19는 모든 의료 관계자에게 큰 관심사가 되고 있습니다. 일반적으로 면역억제제를 복용하는 다발성 경화증(MS) 환자는 만성 질환을 가진 환자의 사망률이 높다는 우려를 표명합니다. 코로나바이러스병-19(COVID-19) 증가는 다발성 경화증 환자(PwMS)에 새로운 과제를 초래합니다. 2022년 1월에 발표된 「다발성 경화증의 치료와 관리에 있어서의 COVID-19의 영향」이라고 표기된 조사에 의한 것이다: 유럽 다발성 경화증 치료 연구 위원회의 조사 결과」에 의하면, 원격 의료는 케어에 대한 제한된 접근을 극복하기 위해 이용되었으며, 새롭게 활성화되거나 널리 실시되었습니다.
또, 2021년에 발표된 다른 연구 논문 「북 이탈리아의 진행성 다발성 경화증 환자 집단에 대한 COVID-19 락 다운의 영향」에서는 락 다운 기간중(2020년 3월-2020년 5월), 대부분의 환자는 MS 센터를 방문하지 않고 원격 의료만으로 스크리닝을 받았습니다. 2020년 6월, MS 센터에 정기적인 방문이 재개되었습니다. COVID-19의 잠금 기간 동안, 많은 진행성 다발성 경화증(pMS) 환자는 신체 활동의 감소와 정기적 인 물리치료를 유지할 수 없기 때문에 신경학적 장애, 불쾌감, 우울증, 체중 증가를 악화시켜야 했습니다. 이러한 발견은 팬데믹(세계적 유행)을 막기 위해 수행 된 공중 보건 대책이 pMS 환자에게 약간 악영향을 미칩니다는 것을 돋보이게합니다.
게다가, 다발성 경화증 환자는 COVID-19의 유행 중에 질병 개질 치료제(DMT)의 복용에 관한 조언이 요구되고 있습니다. 국립 MS 협회와 국립 의료 자문 위원회의 대표는 MS 환자에 대한 국제 다발성 경화증 연합(MSIF)의 세계 COVID-19에 관한 조언을 개정하는 위원회에 참가했습니다. 일부 예비 증거는 인터페론이 COVID-19에 의한 입원의 필요성을 줄일 수 있음을 시사했습니다. 따라서이 증거는 유행 중에 다발성 경화증에 대한 지속적인 약물 요법을 시사했습니다.
다발성 경화증(MS)의 유병률 상승과 같은 요인으로 조사된 시장은 향후 급속한 성장률로 성장할 것으로 예상됩니다. 2020년 12월에 발표된 “Rising prevalence of multiple sclerosis worldwide: 세계에서 280만명(인구 10만명당 35.9명)이 MS 환자인 것으로 추정되고 있습니다. MS의 유병률은 2013년 이후 모두의 지역에서 증가하고 있지만, 유병률 추정치에는 격차가 있습니다. 여성의 MS 환자 수는 남성의 두 배입니다.
또한 MS의 파이프라인 제품에 대한 기업의 관심 증가도 시장의 성장을 뒷받침하고 있습니다. 이 시장의 대기업인 Biogen는 올레라브루티닙의 개발을 진행하고 있으며, 이 제제는 현재 제2상 개발 단계에 있습니다. 또한 2021년 9월 TG Therapeutics는 재발형 다발성 경화증(RMS) 환자에 대한 치료제로서 당사가 개발 중인 당쇄변형 항CD20 단클론항체인 우브리툭시맙의 승인을 요구하는 생물제제 승인 신청(BLA)을 미국 식품의약국(FDA)에 제출했다고 발표했습니다.
위의 기업과 마찬가지로 브리스톨 마이어스 스퀴브 컴퍼니 등 다른 제약 기업도 MS 치료제 개발을 진행하고 있습니다. 이것은 MS 치료제 파이프라인이 예측 기간 동안 연구 시장의 성장을 뒷받침할 가능성을 보여줍니다.
주요 제약 기업도 의약품 개발 프로세스에 많은 투자를 하고 있습니다. 주요 제약 회사는 많은 고객을 수용하기 위해 가능한 한 많은 적응증을 목표로 할 계획입니다. 이 때문에 MS 시장도 혜택을 받고 있습니다. 예를 들어, 다발성 경화증의 치료제로 개발된 것은 재발 관해형 MS, 2차성 진행성 MS, 1차성 진행성 MS, 미엘린 수복 또는 신경보호 등을 포함합니다. 예를 들어, Novartis는 2021년 3월 재발형 다발성 경화증(RMS) 치료제 케심프타(일반명: 오파투무맙)의 유럽 위원회 승인을 받았습니다.
따라서 위의 요인으로 인해 시장은 예측 기간 동안 성장할 것으로 예상됩니다. 그러나 약물과 관련된 부작용과 약물비가 높아 시장 성장을 방해할 수 있습니다.
제1선택제인 주사제를 이용한 전통적인 다발성 경화증(MS) 치료는 널리 적용되었음에도 불구하고 치료 어드레싱과 효능에 대한 가장 큰 우려가 남아 있습니다. MS 치료제로 최근 승인된 신규 경구 약물은 치료에 있어서 큰 진보를 의미합니다. 경구 투여 경로는 환자 만족도를 높이고 치료 규정 준수를 향상시킵니다.
주사 바늘이 약한 사람은 MS 치료에 경구 옵션도 있습니다. 매일 또는 하루에 두 번 복용하는 경구 약물은 정기적 인 투여 일정을 유지해야합니다. 이들은자가 투여가 가장 쉽습니다. 현재 사용 가능한 경구 다발성 경화증 치료제로는 오버지오(테리플루노미드), 길레니아(핑고리모드), 텍피데라(푸마르산디메틸) 등이 있습니다.
2021년 6월 유럽위원회(EC)는 재발 관해형 다발성 경화증(RRMS)의 10-17세 소아 환자의 치료제로서 오버지오(테리플루노미드)를 승인했습니다. 이 승인을 통해 오버지오는 유럽 연합(EU)에서 소아 및 청소년의 다발성 경화증(MS)의 첫 번째 치료제로서 최초의 경구 약물이 됩니다. 또한 2020년 3월 브리스톨 마이어스 스퀴브 컴퍼니는 임상적으로 고립된 증후군, 재발 관해형 질환, 활동성 이차성 진행성 질환을 포함한 성인의 재발형 다발성 경화증(RMS)의 치료제로서 제포시아(오자니모드) 0.92mg의 미국 식품의약국(FDA)의 승인을 취득했습니다. 제포시아는 하루에 한 번 복용하는 경구 약물입니다. 따라서 다발성 경화증의 치료를위한 혁신적인 경구 약물의 승인과 출시는 이 부문의 성장을 가속합니다.
COVID-19 팬데믹은 팬데믹 중 다발성 경화증 환자의 치료에 심각한 영향을 미쳤습니다. 2020년 12월에 발표된 "Impact of COVID-19 on the United States and Canadian neurologists'therapeutic approach to multiple sclerosis: a survey of knowledge, attitudes, and practices(미국 및 캐나다 신경과 의사의 다발성 경화증에 대한 COVID-19의 영향: 지식, 태도, 실천에 관한 조사)”라는 제목의 조사 결과에 따르면 환자 수는 평균 79% 감소했습니다. 23%가 COVID-19를 두려워하여 DMT를 자가중단하는 환자를 인식하고 있으며, 43%는 의학적 조언에 반하여 그렇게 하고 있는 것으로 추정되었습니다. 또한 2021년에 발표된 "구미에서 재발관해형 다발성 경화증(RRMS) 환자와 신경내과의사의 진찰에 있어서의 COVID-19의 영향"에 관한 다른 연구에서는 2020년 2분기에 미국( 미국)의 응답자 중 RRMS 환자가 신경내과의사를 직접 만난 것으로 응답한 것은 31%였는데, 진찰이 전화로 이루어진 경우는 19%, 원격 의료에서는 42%, 인터넷 경유로는 68%였습니다. 2020년 4분기까지 미국에서는 RRMS 환자가 직접 진찰하는 비율이 68%로 크게 증가하는 것으로 보고되었습니다.
다발성 경화증 치료제 시장은 북미에서 높은 성장이 예상됩니다. 미국은 Biogen, Novartis AG, Sanofi SA 등 주요 시장입니다. 따라서 이러한 기업들은 이 시장 조사에서 신약의 확립에 주력하고 있으며 이 지역의 성장에 기여하고 있습니다.
또한, 2020년 9월에 출판된 Atlas of Multiple Sclerosis, 3rd Edition에 따르면, 아메리카에서 다발성 경화증의 유병률은 100,000명당 112명입니다. 북미에서 이러한 다발성 경화증의 높은 유병률은 시장 성장을 가속할 것으로 예상됩니다.
또한 규제 당국의 승인도 시장 성장을 뒷받침하고 있습니다. 예를 들어, 2020년 8월, Novartis는 재발성 다발성 경화증(RMS) 치료를 위한 피하주로 케심프타(Ofatummab, 구명 OMB157)의 미국 식품의약국(FDA) 승인을 받았습니다. 케심프타는 센소레이디 자동 주사 펜을 사용하여 집에서월1회 자가 투여할 수 있는 최초의 B 세포 치료제입니다.
이상으로부터, 북미의 다발성 경화증 치료제 시장이 시장의 성장을 견인할 것으로 기대되고 있습니다.
다발성 경화증 치료제 시장은 진출기업이 적기 때문에 통합되어 있습니다. 이 회사는 다발성 경화증의 파이프라인 의약품에 주력하는 주요 제약 회사입니다. 제약업계에서 R&D 투자가 증가함에 따라 앞으로 더 많은 기업들이 이 시장에 진입하여 경쟁이 치열해질 가능성이 있다고 생각됩니다.
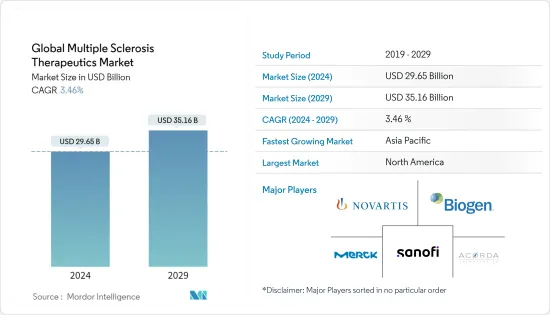
The Global Multiple Sclerosis Therapeutics Market size is estimated at USD 29.65 billion in 2024, and is expected to reach USD 35.16 billion by 2029, growing at a CAGR of 3.46% during the forecast period (2024-2029).
COVID-19 has become a big concern for medical professionals across the board. Patients with multiple sclerosis (MS), commonly on immunosuppressive medicines, have expressed concern about the higher mortality rate among patients with chronic conditions. The rise of Coronavirus disease-19 (COVID-19) creates new challenges for patients with multiple sclerosis (PwMS). As per the research study published in January 2022 titled 'Impact of COVID-19 on multiple sclerosis care and management: Results from the European Committee for Treatment and Research in Multiple Sclerosis survey', Telemedicine was used to overcome the limited access to care and was newly activated or widely implemented.
Also, in another research article published in 2021 on 'Impact of COVID-19 lockdown on a population of progressive multiple sclerosis patients in Northern Italy', during the lockdown period (March 2020-May 2020), most patients were solely screened via telemedicine rather than being visited at the MS Center. In June 2020, regular visits to the MS Center were resumed. During the Covid-19 lockdown, many Progressive Multiple Sclerosis (pMS) patients had to deteriorate neurological disability, weariness, depression, and weight gain, likely due to reduced physical activity and the inability to maintain regular physiotherapy. These findings highlight the slight negative impact of public health measures implemented to contain the pandemic on pMS patients.
Furthermore, MS patients have requested advice on taking disease-modifying treatments (DMTs) during the COVID-19 epidemic. Representatives of the National MS Society and the National Medical Advisory Committee participated in a committee to revise the Multiple Sclerosis International Federation (MSIF) global COVID-19 advice for people living with MS. Some preliminary evidence suggested that interferons may reduce the need for hospitalization due to COVID-19. Hence, the evidence suggested continuous medications for multiple sclerosis during the pandemic.
The market studied is expected to witness a rapid growth rate in the future, owing to factors such as the rising prevalence of multiple sclerosis (MS). As per the study published in December 2020 titled 'Rising prevalence of multiple sclerosis worldwide: Insights from the Atlas of MS, third edition,' A total of 2.8 million people are estimated to live with MS worldwide (35.9 per 100,000 population). MS prevalence has increased in every region since 2013, but gaps in prevalence estimates persist. The pooled incidence rate across 75 reporting countries was 2.1 per 100,000 persons/year, and the mean age of diagnosis was 32years. Females are twice as likely to live with MS as males.
Besides, the growing focus of companies on pipeline products for MS is also boosting the market growth. Biogen, a leading player in the market, has been developing Orelabrutinib, which is currently in phase II of development; similarly, Novartis has been developing remibrutinib, which is in Phase III. Also, in September 2021, TG Therapeutics announced the submission of a Biologics License Application (BLA) to the U.S. Food and Drug Administration (FDA) requesting approval of ublituximab, the Company's investigational glycoengineered anti-CD20 monoclonal antibody, as a treatment for patients with relapsing forms of multiple sclerosis (RMS).
Similar to the companies mentioned above, other pharmaceutical players, such as Bristol-Myers Squibb Company, have been developing drugs for MS. This indicates that pipeline drugs for MS may boost the studied market's growth in the forecast period.
Big pharmaceutical companies have also been investing heavily in the drug development process. They are planning to target as many indications as possible to cater to a large number of customers. Owing to this, the MS market has also been benefiting. For instance, the drugs developed for multiple sclerosis include Relapsing-remitting MS, Secondary progressive MS, Primary progressive MS, and Myelin repair or neuroprotection. For Instance, in March 2021, Novartis received European Commission approval for Kesimpta (ofatumumab) for treating relapsing forms of multiple sclerosis (RMS) in adults with active disease defined by clinical or imaging features.
Thus, owing to the abovementioned factors, the market is expected to project growth over the forecast period. However, side effects associated with medications and the high cost of drugs may hinder the growth of the market.
Classical multiple sclerosis (MS) treatments using first-line injectable drugs, despite being widely applied, remain a foremost concern regarding therapeutic adherence and efficacy. Novel oral drugs recently approved for treating MS represent significant advances in therapy. The oral route of administration supports patient satisfaction and increases therapeutic compliance.
If someone is uncomfortable with needles, oral options are also available for treating MS. Taken daily or twice daily; oral medications require one to maintain a regular dosing schedule. These are the easiest to self-administered. The currently available oral multiple sclerosis drugs include Aubagio (teriflunomide), Gilenya (fingolimod), and Tecfidera (dimethyl fumarate).
In June 2021, The European Commission (EC) approved Aubagio (teriflunomide) for the treatment of pediatric patients 10 to 17 years of age with relapsing-remitting multiple sclerosis (RRMS). The approval confirms Aubagio as the first oral multiple sclerosis (MS) therapy for first-line treatment of children and adolescents with MS in the European Union. Also, in March 2020, Bristol-Myers Squibb Company received United States Food and Drug Administration approval for ZEPOSIA (ozanimod) 0.92 mg for the treatment of adults with relapsing forms of multiple sclerosis (RMS), including clinically isolated syndrome, relapsing-remitting disease, and active secondary progressive disease. ZEPOSIA is an oral medication taken once daily. Hence, approval and launch of innovative oral medicines for the treatment of multiple sclerosis are driving segmental growth.
The COVID-19 pandemic has severely impacted the care of patients living with Multiple Sclerosis during the pandemic. As per the research study published in December 2020 titled 'Impact of COVID-19 on the United States and Canadian neurologists' therapeutic approach to multiple sclerosis: a survey of knowledge, attitudes, and practices', patient volume decreased by an average of 79%. 23% were aware of patients self-discontinuing a DMT due to fear of COVID-19, with 43% estimated to be doing so against medical advice. Also, in another study published in 2021 on 'The impact of COVID-19 on consultations between relapsing-remitting multiple sclerosis (RRMS) patients and their neurologists in Europe and United States', in Q2 2020, 31% of United States (US) respondents reported that RRMS patients saw their neurologist in person as compared to 19% where the consultation was conducted by phone, 42% by telemedicine and 68% via internet. By Q4 2020, the proportion of reported RRMS patients in person significantly increased to 68% in the US.
The market for multiple sclerosis therapeutics is expected to show high growth in the North American region, which is majorly attributed to the presence of key players and the rising prevalence of the disease in this region. The United States is the primary market for companies such as Biogen, Novartis AG, and Sanofi SA, among others. Therefore, these companies have been focusing more on establishing their new drugs in this market study, contributing to this region's growth.
Furthermore, as per the Atlas of Multiple Sclerosis, 3rd Edition, published in September 2020, the prevalence of multiple sclerosis in the Americas is 112 per 100,000. Such a high prevalence of multiple sclerosis in North America is expected to drive the growth of the market.
Additionally, the approval by the regulatory authorities is also propelling the growth of the market. For Instance, in August 2020, Novartis received United States Food and Drug Administration approval for Kesimpta (ofatumumab, formerly OMB157) as an injection for subcutaneous use for the treatment of relapsing forms of multiple sclerosis (RMS). Kesimpta is the first B-cell therapy that can be self-administered once monthly at home via the Sensoready autoinjector pen.
Thus, owing to the abovementioned the North American multiple sclerosis therapeutics market is expected to drive the growth of the market.
The market for Multiple sclerosis therapeutics is consolidated, as there are few players in this market. These companies are the big pharmaceutical companies focusing on pipeline drugs for multiple sclerosis. With the rising R&D investment in the pharmaceutical industry, it is believed that more companies may enter the market studied in the future, and the competition may increase.